题目内容
【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO![]() 2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/mol/L | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO)/mol/L | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H______0(填写“>”、“<”、“=”。
(2)前2s内的平均反应速率v(N2)=_____________。
(3)在该温度下,反应的平衡常数K=______________。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是_____。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
实验编号 | T/℃ | NO初始浓度mol/L | CO初始浓度mol/L | 催化剂的比表面积m2/g |
Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
Ⅱ | 124 | |||
Ⅲ | 350 | 124 |
①请在上表格中填入剩余的实验条件数据________________。
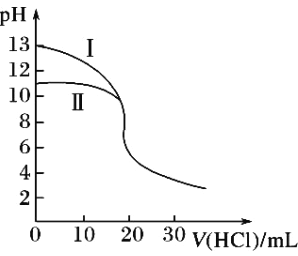
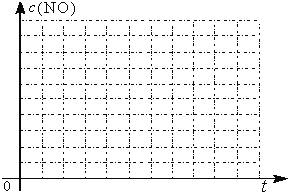
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号________________。
【答案】< 1.88×10-4mol/(L·s) 5000 C、D II: 280、1.20×10-3、5.80×10-3,Ⅲ:1.2×10-3、5.80×10-3 
【解析】
(1)根据反应能够自发进行,利用△H-T△S<0来分析该反应的焓变;
(2)根据化学反应速率的定义及2s内浓度的变化量来计算解答;
(3)根据该温度下达化学平衡时各物质平衡时浓度及化学平衡常数的概念来计算;
(4)能提高NO转化率则化学平衡正向移动,利用影响化学平衡移动的因素来分析;
(5)根据实验目的验证温度、催化剂比表面积对化学反应速率的影响规律,则应保证浓度相同,然后相同温度时比较催化剂比表面积,相同催化剂比表面积时比较温度,然后利用影响化学反应速率及化学平衡的因素来分析图象。
(1)因该反应2NO+2CO![]() 2CO2+N2中气体减少,则△S<0非自发,由反应能够自发进行,则△H-T△S<0,即该反应一定是放热才有可能自发进行,放热反应的△H<0,故答案为:<;
2CO2+N2中气体减少,则△S<0非自发,由反应能够自发进行,则△H-T△S<0,即该反应一定是放热才有可能自发进行,放热反应的△H<0,故答案为:<;
(2)由表格中的数据可知2s内NO浓度的变化量为1.00×10-3-2.50×10-4=7.50×10-4 mo/L,则υ(NO)=![]() =3.75×10-4 mol/(L·s),由化学反应速率之比等于化学计量数之比,则υ(N2)=
=3.75×10-4 mol/(L·s),由化学反应速率之比等于化学计量数之比,则υ(N2)=![]() υ(NO)≈1.88×10-4 mol/(L·s),故答案为:1.88×10-4 mol/(L·s);
υ(NO)≈1.88×10-4 mol/(L·s),故答案为:1.88×10-4 mol/(L·s);
(3)由表格中的数据可知到4s时达到化学平衡,则
则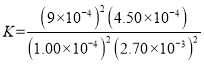 =5000,故答案为:5000;
=5000,故答案为:5000;
(4)催化剂不影响平衡的移动,A项错误;
该反应放热,故降温平衡正向移动,NO转化率增大,B项错误;
该反应放热,故降温平衡正向移动,NO转化率增大,C项正确;
缩小体积,即增大压强,平衡向体积减小的方向运动,即正向移动,D项正确。
故答案为:CD;
(5) ①因Ⅰ、Ⅱ比表面积不同,则应控制温度相同,所有浓度应控制相同来验证催化剂比表面积对速率的影响;Ⅱ、Ⅲ比表面积相同,温度不同,则所有浓度应控制相同来验证反应温度对速率的影响,故答案为280;1.20×10-3;5.80×10-3;1.20×10-3;5.80×10-3;
②因Ⅰ、Ⅱ温度相同,催化剂对平衡移动无影响,则平衡不移动,但Ⅱ的速率大,则Ⅱ先达到化学平衡,Ⅰ、Ⅱ达平衡时NO的浓度相同;而Ⅲ的温度高,则反应速率最大且平衡逆移,即达到化学平衡时c(NO)增大,故答案为 。
。

【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向FeBr2溶液中通入适量Cl2,溶液由浅绿色变为黄色 | Cl2氧化性强于Br2 |
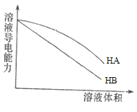
B | 常温下,等体积pH=3的HA和HB两种酸分别加水稀释,溶液导电能力如图
| HA酸性比HB弱 |
C | 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 | X具有氧化性 |
D | 取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体 | 气体为氧气 |
A.AB.BC.CD.D
【题目】下列有关物质检验的实验结论正确的是
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有 |
B | 向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
D | 将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热后有银镜生成 | 该物质一定属于醛类 |
A.AB.BC.CD.D