题目内容
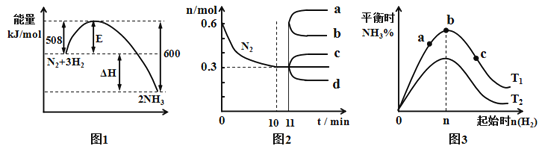
【题目】合成氨反应为:N2(g)+3H2(g)![]() 2NH3(g).图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线.图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.下列说法正确的是
2NH3(g).图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线.图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.下列说法正确的是
A.由图1可知2NH3(g)![]() N2(g)+3H2(g) △H=-92kJ·mol-1
N2(g)+3H2(g) △H=-92kJ·mol-1
B.图2中0~10min内该反应的平均速率v(H2)=0.09mol·L-1·min-1
C.图2中从11min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为d
D.图3中温度T1<T2,a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点
【答案】C
【解析】
试题分析:A、由图1知,氮气和氢气的能量大于氨气的能量,所以由氮气和氢气生成氨气是放热反应,氨气分解是吸热反应,A错误;B、v(N2)=![]() =0.015molL-1min-1,v(H2)=3v(N2)=0.045molL-1min-1,B错误;C、当缩小容器的体积,气体的压强增大,导致平衡向气体体积减小的方向移动,即向正反应方向移动,氮气的物质的量减少,所以曲线d符合,C正确;D、相同温度下,一定量氮气时,氢气的浓度越大,平衡向正反应方向移动导致氮气的转化率越大,所以图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c点,D错误;答案选C。
=0.015molL-1min-1,v(H2)=3v(N2)=0.045molL-1min-1,B错误;C、当缩小容器的体积,气体的压强增大,导致平衡向气体体积减小的方向移动,即向正反应方向移动,氮气的物质的量减少,所以曲线d符合,C正确;D、相同温度下,一定量氮气时,氢气的浓度越大,平衡向正反应方向移动导致氮气的转化率越大,所以图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c点,D错误;答案选C。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案【题目】现有部分元素的性质、用途与原子(或分子)结构如表所示:
元素编号 | 元素性质与原子(或分子)结构 |
W | 周期表中原子半径最小的元素 |
X | 氢化物可与其最高价氧化物的水化物反应生成盐 |
Y | 一种核素在考古时常用来鉴定一些文物的年代 |
Z | M层比K层少1个电子 |
T | 存在两种同素异形体,其中一种可吸收紫外线 |
(1)元素Y在周期表中的位置第____,元素T的简单离子结构示意图_____。
(2)W、X、Z、T中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式____________。
(3)元素W与元素X、T可以分别形成多种核外电子总数为10的微粒,其中有四种微粒可以发生反应:甲 + 乙 ![]() 丙 + 丁,该反应为:_____________。
丙 + 丁,该反应为:_____________。
(4)元素X与元素W以原子个数比1∶2化合形成常用于火箭燃料的化合物戊,元素T和元素W以原子个数比为1∶1化合形成化合物己,戊与己能发生氧化还原反应,生成X单质和另一种液体化合物,写出该反应的化学方程式________。