��Ŀ����
��1������ɸ÷�Ӧ�����ӷ���ʽ��
C + MnO4- + H+ �� CO2��+ Mn2+ + H2O
��2������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������С����з�ӦCO(g ) + H2O(g) CO2(g) + H2(g)�õ������������ݣ�
CO2(g) + H2(g)�õ������������ݣ�
��ʵ��1�ӿ�ʼ���ﵽ��ѧƽ��ʱ����v��CO2����ʾ�ķ�Ӧ����Ϊ ������ȷ��0.01��
�ڸ÷�ӦΪ ��������š����ȷ�Ӧ��ʵ��2�д�ƽ��ʱ CO��ת����Ϊ ��
��3�����ݻ��ɱ���ܱ������з�����Ӧ��mA(g) + nB(g) pC(g) ,��һ���¶ȺͲ�ͬѹǿ�´ﵽƽ��ʱ���ֱ�õ�A�����ʵ���Ũ�����±�
pC(g) ,��һ���¶ȺͲ�ͬѹǿ�´ﵽƽ��ʱ���ֱ�õ�A�����ʵ���Ũ�����±�
�ٵ�ѹǿ��2��105 Pa���ӵ�5��105 Paʱ��ƽ�� �ƶ�������� ���� ������
�ڵ�ѹǿ��5��105 Pa���ӵ�1��106 Paʱ���÷�Ӧƽ�ⳣ������ʽΪK= ������25���£���Ũ��Ϊ0.1mol��L-1��FeCl3��Һ����μ��백ˮ��������ҺpHΪ 5ʱ����Һ��c��Fe3+��Ϊ mol/L ������֪25��ʱ Ksp[Fe(OH)3]=4��10-38��
C + MnO4- + H+ �� CO2��+ Mn2+ + H2O
��2������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������С����з�ӦCO(g ) + H2O(g)
 CO2(g) + H2(g)�õ������������ݣ�
CO2(g) + H2(g)�õ������������ݣ�| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
��ʵ��1�ӿ�ʼ���ﵽ��ѧƽ��ʱ����v��CO2����ʾ�ķ�Ӧ����Ϊ ������ȷ��0.01��
�ڸ÷�ӦΪ ��������š����ȷ�Ӧ��ʵ��2�д�ƽ��ʱ CO��ת����Ϊ ��
��3�����ݻ��ɱ���ܱ������з�����Ӧ��mA(g) + nB(g)
 pC(g) ,��һ���¶ȺͲ�ͬѹǿ�´ﵽƽ��ʱ���ֱ�õ�A�����ʵ���Ũ�����±�
pC(g) ,��һ���¶ȺͲ�ͬѹǿ�´ﵽƽ��ʱ���ֱ�õ�A�����ʵ���Ũ�����±�| ѹǿp/Pa | 2��105 | 5��105 | 1��106 |
| c(A)/mol��L-1 | 0.08 | 0.20 | 0.44 |
�ٵ�ѹǿ��2��105 Pa���ӵ�5��105 Paʱ��ƽ�� �ƶ�������� ���� ������
�ڵ�ѹǿ��5��105 Pa���ӵ�1��106 Paʱ���÷�Ӧƽ�ⳣ������ʽΪK= ������25���£���Ũ��Ϊ0.1mol��L-1��FeCl3��Һ����μ��백ˮ��������ҺpHΪ 5ʱ����Һ��c��Fe3+��Ϊ mol/L ������֪25��ʱ Ksp[Fe(OH)3]=4��10-38��
��1����5 C + 4 MnO4- + 12 H+ = 5 CO2��+ 4 Mn2+ + 6 H2O
��2����0.13 mol��L-1 ��min-1; �ڷ� ; 20%
��3���ٲ�; �� .
.
��4��4��10-11
��2����0.13 mol��L-1 ��min-1; �ڷ� ; 20%
��3���ٲ�; ��
 .
. ��4��4��10-11
�����������1���ٷ�Ӧ��MnO4����Mn2������Ԫ�ػ��ϼ���+7�۽���Ϊ+2�ۣ�������5�ۣ�C��CO2��̼Ԫ�ػ��ϼ���0������Ϊ+4��������4�ۣ����ϼ���С������Ϊ20����MnO4��ϵ��Ϊ4��Cϵ��Ϊ5���ٸ���Ԫ���غ��֪Mn2��ϵ��Ϊ4��CO2ϵ��Ϊ5�����ݵ���غ��֪H��ϵ��Ϊ12��������Ԫ���غ��֪H2Oϵ��Ϊ6����ƽ�����ӷ���ʽΪ5 C + 4 MnO4- + 12 H+ ="=" 5 CO2��+ 4 Mn2+ + 6 H2O���𰸣�5 C + 4 MnO4- + 12 H+ ="=" 5 CO2��+ 4 Mn2+ + 6 H2O��
��2���١��ɱ������ݿ�֪��CO�����ʵ����仯��Ϊ4mol-2.4mol=1.6mol��v��CO��=
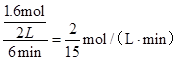 ������֮�ȵ��ڻ�ѧ������֮�ȣ���v��CO2��=v��CO��=
������֮�ȵ��ڻ�ѧ������֮�ȣ���v��CO2��=v��CO��= mol/��L��min��=0.13mol/��L��min����
mol/��L��min��=0.13mol/��L��min�����ʴ�Ϊ��0.13mol/��L��min����
�ڡ�ʵ��1��CO��ת����Ϊ��100%=40%��ʵ��2��CO��ת����Ϊ��100%=20%����ʵ��1��ת���ʴ���ʵ��2����˵���¶�����ƽ�����淴Ӧ�����ƶ�������Ӧ���ȣ�
�ʴ�Ϊ�����ȣ�
ƽ��ʱCO�����ʵ���Ϊ1.6mol����
CO��g��+H2O��g��
 CO2��g��+H2��g����
CO2��g��+H2��g������ʼ��mol����2 1 0 0
�仯��mol����0.4 0.4 0.4 0.4
ƽ�⣨mol����1.6 0.6 0.4 0.4
ʵ��2�д�ƽ��ʱ CO��ת����Ϊ
 ��100%=20%
��100%=20%�𰸣���0.13 mol��L-1 ��min-1; �� �� ; 20%
��3�� ��ѹǿ��2��105Pa���ӵ�5��105 Paʱ��A��Ũ��Ӧ�仯Ϊ0.08mol��L��1��2.5����Ϊ0.20mol��L��1����ͼ���б仯Ϊ0.20mol��L��1��˵��ƽ�ⲻ�ƶ�����ѹʱ������AŨ������ı�������ѹǿ����ı�����
��ѹǿ��2��105 Pa ���ӵ�1��106 Paʱ��A��Ũ��Ӧ�仯Ϊ0.08mol��L��1��5����0.40mol��L��1����ͼ����A��Ũ��Ϊ0.44mol��L��1��˵��ƽ��������У����ݢٿ�֪��Ӧ�������������ķ�Ӧ�����Դ�ʱB��ѹ��ΪҺ�����壬��ѹǿ��5��105 Pa���ӵ�1��106 Paʱ���÷�Ӧƽ�ⳣ������ʽΪK=

�ʴ�Ϊ���ٲ�; ��
 .
. ��4
 ���𰸣�4��10-11
���𰸣�4��10-11
��ϰ��ϵ�д�
�����Ŀ
 ��������10mol/L����Һ����ȣ��������������к�ɫ�������� �ڲ����̼�����ζ������ ����Һ������ɫ���ݴ��ж�����˵����ȷ����
��������10mol/L����Һ����ȣ��������������к�ɫ�������� �ڲ����̼�����ζ������ ����Һ������ɫ���ݴ��ж�����˵����ȷ����
 2HCOOH+O2������˵����ȷ����
2HCOOH+O2������˵����ȷ����