��Ŀ����
����Ŀ��NiS �������մɺ��´ɵ���ɫ����NiS ����ˮ����ʱ�ܱ�����������Ni(OH)S����H2Sͨ��ϡ�����ữ��NiSO4��Һ�У��������ˣ��Ƶ�NiS ������װ����ͼ��ʾ:

���ж�ʵ���������ȷ����
A. ��װ��A�еμ�����ˮǰͨ��N2����Ϊ�˽�H2S����C װ������NiSO4��Һ��Ӧ
B. װ��B ��ʢ��Ũ����
C. װ��D �е�ϴ��ҺӦ����й�������ˮ
D. ��Ӧ���������ͨ��N2 �ɽ�Cװ���в����ij���ѹ����˳���©����
���𰸡�C
��������A. NiS����ˮ����ʱ�ܱ�����������Ni(OH)S����װ��A�еμ�����ˮǰͨ��N2����Ϊ�˽���ȥװ���еĿ�������A����B. �����ܹ���Ũ������������B���� C. NiS����ˮ����ʱ�ܱ�����������Ni(OH)S��Ϊ�˷�ֹ��������װ��D�е�ϴ��ҺӦ����й�������ˮ����C��ȷ��D. ��Ӧ���������ͨ��N2�ɽ�Cװ���в�����H2S�ϳ����գ���ֹ��Ⱦ��������D����ѡC��

 ����С����ͬ������ϵ�д�
����С����ͬ������ϵ�д�����Ŀ��������p��Ԫ�ع���13�֣�������ȫ���Ƿǽ���Ԫ�ء�
(1)��̬��ԭ�ӵļ۲�����Ų�ͼΪ_______________��������p��Ԫ���У���һ��������С��Ԫ����縺������Ԫ����ɵĻ�������_______________(�ѧʽ)��
(2)±�����𡢵������γ�BF3��NCl3��PBr3�������й��������ַ��ӵ�������ȷ����_________��
A.��ѧ��������ͬ B.�ռ乹����ͬ
C.����ԭ�ӵ��ӻ����������ͬ D.����ԭ�ӵļ۲���Ӷ�����ͬ
(3)CS2��һ���ܼ��������ܽ���ǡ�д��һ����CS2������ͬ�ռ乹�ͺͼ�����ʽ�ķ��ӻ�����______________��CO����Ni�γ����������͵������Ni(CO)4��3.42gNi(CO)4�к���_____mol�Ҽ���
(4)CCl4��ˮ�������ܣ�SiCl4��CCl4���ӽṹ���ƣ�����ˮ������ˮ�ⷴӦ�����¶������ʲ�ͬ��ԭ����________________��
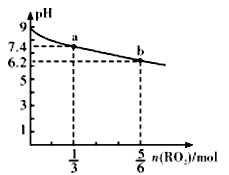
(5)���ļ���±������۵����£�
±���� | AlF3 | AlCl3 | AlBr3 | AlI3 |
�۵�/�� | 1040 | 190 | 97.5 | 191 |
AlBr3�ľ���������______��AlI3�����д��ڵ���������_______________��
(6)����������Ϊԭ��Ʒ�壬��һ���������ǽ������ϣ��侧���ܶ�Ϊ��g/cm3��������ͼ��ʾ��
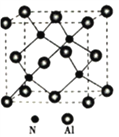
����ԭ�ӵ���λ��Ϊ_______________��
����NAΪ�����ӵ�������ֵ�������������У���ԭ�Ӻ͵�ԭ��֮����̵ĺ˼��Ϊ________nm��