题目内容
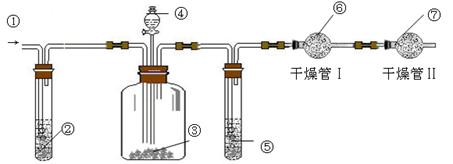
(14分)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)装置①是氯气发生装置,圆底烧瓶中盛放MnO2固体,其反应的化学方程式为 。
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
A.NaBiO3 B.FeCl3 C.PbO2
(已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>FeCl3)
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是① ; ② 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是 (填写编号字母);从②的试管中分离出该晶体的方法是 (填写实验操作名称)。
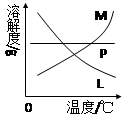
(5)一定量的氢气在氯气中燃烧,所得的混合物用100mL 3.00mol/L的NaOH溶液(密度为1.2g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。所得溶液中Cl-离子的物质的量 。

图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)装置①是氯气发生装置,圆底烧瓶中盛放MnO2固体,其反应的化学方程式为 。
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
A.NaBiO3 B.FeCl3 C.PbO2
(已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>FeCl3)
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是① ; ② 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是 (填写编号字母);从②的试管中分离出该晶体的方法是 (填写实验操作名称)。
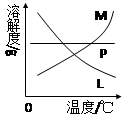
(5)一定量的氢气在氯气中燃烧,所得的混合物用100mL 3.00mol/L的NaOH溶液(密度为1.2g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。所得溶液中Cl-离子的物质的量 。
(每空2分,共14分)
(1)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O (2)A、C
MnCl2+Cl2↑+2H2O (2)A、C
(3)①制取温度不同; ②制取时碱的浓度也不同 (4)M 过滤
(5)0. 250mol
(1)MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O (2)A、C
MnCl2+Cl2↑+2H2O (2)A、C (3)①制取温度不同; ②制取时碱的浓度也不同 (4)M 过滤
(5)0. 250mol
试题分析:该实验的目的是制取氯酸钾、次氯酸钠和探究氯水的性质,①制取氯气的装置;②是制取氯酸钾装置;③是制取此氯酸钠装置;④验证氯水的漂白性;⑤吸收氯气的装置。
(1)实验室制氯气一般用二氧化锰和浓盐酸加热制取,方程式为MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;(2)二氧化锰作氧化剂,能代替二氧化锰的必须具有强氧化性,同时氧化性要比氯气的氧化性强,氯化铁的氧化性比氯气弱,不能制取氯气,故选A、C。
(3)②的试管里盛有30% KOH溶液,并置于热水浴中;③的试管里盛有8% NaOH溶液,并置于冰水浴中;可以看出前者温度高,同时碱的浓度大,而后者反应在低温下,同时浓度小;
(4)冷却析出大量晶体,说明溶解度随温度变化很大,同时温度越低,溶解度越小,根据图像可以看出,选择M,分离溶液中的固体物质,一般用过滤的方法。
(5)NaOH为0.3mol,全部转化为氯化钠和次氯酸钠,根据原子守恒知道氯原子的物质的量等于钠原子的物质的量,则n(Cl-)="0.3-0.05=0." 250mol
点评:本题综合性较强,通过信息的给予,还考查学生的读取信息,运用信息的能力,属于中等难度习题。

练习册系列答案
相关题目