题目内容
18.“纳米材料”是指粒子直径在几纳米到几十纳米的材料.如将“纳米材料”分散在液体分散剂中,所得混合物具有的性质是( )| A. | 所得物质一定为悬浊液 | B. | 所得物质一定为乳浊液 | ||
| C. | 肯定有丁达尔效应 | D. | 所得物质肯定不能能透过滤纸 |
分析 由“纳米技术”是指粒子直径在几纳米到几十米的材料,则分散到液体分散剂中,分散质的直径在1nm~100nm之间,以此来解答.
解答 解:分散系中分散质的直径在1nm~100nm之间的属于胶体分散系,
由“纳米技术”是指粒子直径在几纳米到几十米的材料,则分散到液体分散剂中,分散质的直径在1nm~100nm之间,则该混合物属于胶体.
A.该混合物属于胶体,不是浑浊液,故A错误;
B.该混合物属于胶体,不是乳浊液,故B错误;
C.该混合物属于胶体,胶体能发生丁达尔效应,故C正确;
D.该混合物属于胶体,胶体能透过滤纸,故D错误;
故选C.
点评 本题考查分散系的判断及胶体的性质,明确纳米材料的直径是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
8.根据要求完成下列各小题实验目的.(a、b为弹簧夹,加热及固定装置已略去)
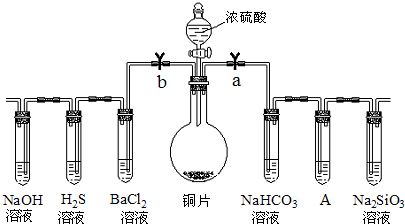
(1)验证碳、硅非金属性的相对强弱.(已知酸性:亚硫酸>碳酸)
①接仪器并检查装置气密性、加药品后,打开a关闭 b,然后滴入浓硫酸,加热.
②铜与浓硫酸反应的化学方程式是:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑.
装置A中的试剂可以是:品红溶液.
③能说明碳的非金属性比硅强的实验现象是:A中品红没有褪色,盛有Na2SiO3溶液的试管中出现白色沉淀.
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性.
①打开b,关闭a.
②H2S溶液中有浅黄色浑浊出现,化学方程式是:2H2S+SO2=3S↓+2H2O
③BaCl2溶液中无明显现象,将其分成两份,分別滴加下列溶液,将产生的沉淀的化学式填人下表相应位置:
写出SO2与氯水反应的离子方程式Cl2+SO2+2H2O=SO42-+4H++2Cl-.

(1)验证碳、硅非金属性的相对强弱.(已知酸性:亚硫酸>碳酸)
①接仪器并检查装置气密性、加药品后,打开a关闭 b,然后滴入浓硫酸,加热.
②铜与浓硫酸反应的化学方程式是:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑.
装置A中的试剂可以是:品红溶液.
③能说明碳的非金属性比硅强的实验现象是:A中品红没有褪色,盛有Na2SiO3溶液的试管中出现白色沉淀.
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性.
①打开b,关闭a.
②H2S溶液中有浅黄色浑浊出现,化学方程式是:2H2S+SO2=3S↓+2H2O
③BaCl2溶液中无明显现象,将其分成两份,分別滴加下列溶液,将产生的沉淀的化学式填人下表相应位置:
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | BaSO4 | BaSO3 |
9.将铝粉投入到下列溶液中,能观察到有气体产生的是( )
| A. | 自来水 | B. | 氯化钠溶液 | C. | 浓氢氧化钠溶液 | D. | 稀氨水 |
6.下列实验用来证明SO2的存在,其中正确的是( )
| A. | 能使品红褪色,加热后又出现红色 | |
| B. | 能使湿润的蓝色石蕊试纸变红 | |
| C. | 通入足量的NaOH溶液中,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸 | |
| D. | 通入稀溴水中能使溴水褪色,得澄清溶液,再滴加Ba(NO3)2溶液有白色沉淀生成,且该沉淀不溶于硝酸 |
13.下列反应中,水既不是氧化剂,也不作还原剂的氧化还原反应是( )
| A. | Na和H2O | B. | Mg 和H2O | C. | CO2和H2O | D. | Na2O2 和H2O |
3.下列叙述正确的是( )
| A. | 光导纤维的主要原料就是Na2SiO3 | |
| B. | 盛液溴的试剂瓶常加少量水 | |
| C. | 硅酸可由SiO2直接制得 | |
| D. | 氯气可用于漂白,这是氯气具有漂白作用 |
10.下列实验操作错误的是( )
| A. |  从滴瓶里倾倒液体 | B. |  从滴瓶里取出液体 | ||
| C. |  向试管里加入粉末 | D. |  给试管里液体加热 |
7.按硫元素的化合价由低到高的顺序排列的物质为:KHS、S、M、Al2(SO4)3、,其中物质M可能是( )
| A. | H2S | B. | Na2SO4 | C. | SO3 | D. | SO2 |