题目内容
(15分)已知:在实验中,常常利用高沸点酸制低沸点酸。以六水合氯化镁(MgCl2·6H2O)为原料制备无水氯化镁。已知MgCl2·6H2O晶体在空气中加热时,释放出部分结晶水,同时生成Mg(OH)Cl或MgO;在干燥HCl气流中加热,能制得无水MgCl2。
可选用药品:MgCl2·6H2O晶体、NaCl(s)、KClO3(s)、MnO2、浓H2SO4、浓盐酸、稀NaOH溶液。
 仪器如图所示(装置可重复使用)。回答下列问题:
仪器如图所示(装置可重复使用)。回答下列问题:

(1)组装氯化氢气体发生器,应选用的仪器(用编号A、B等填入)是 ,
有关的化学方程式是 。
(2)按气流方向,其余装置的连接顺序(用数字①、②等填入)是:
( )→( )( )→( )( )→( )( )
(3)各装置中应放的药品: B.______,D.______,E.______。
(4)B装置的作用是_________________。
(5)从实验安全角度考虑,上述所给药品和仪器设计的实验存在不足,请你提出修改建议: 。
可选用药品:MgCl2·6H2O晶体、NaCl(s)、KClO3(s)、MnO2、浓H2SO4、浓盐酸、稀NaOH溶液。
 仪器如图所示(装置可重复使用)。回答下列问题:
仪器如图所示(装置可重复使用)。回答下列问题:
(1)组装氯化氢气体发生器,应选用的仪器(用编号A、B等填入)是 ,
有关的化学方程式是 。
(2)按气流方向,其余装置的连接顺序(用数字①、②等填入)是:
( )→( )( )→( )( )→( )( )
(3)各装置中应放的药品: B.______,D.______,E.______。
(4)B装置的作用是_________________。
(5)从实验安全角度考虑,上述所给药品和仪器设计的实验存在不足,请你提出修改建议: 。
(1)C、E(2分) 2 NaCl+H2SO4(浓)
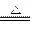 Na2SO4+2HCl↑(3分)
Na2SO4+2HCl↑(3分)(2)⑤①②⑥⑦④③(3分)(3)稀NaOH MgCl2·6H2O 浓H2SO4(3分)
(4)吸收多余HCl气体,防止环境污染(2分)
(5)在B中加入一定量的四氯化碳浸没导管口或用盛装碱石灰的干燥管代替B装置或在B的进气管口接一下倒置的漏斗,接近液面(2分)
(1)实验室可以利用氯化物固体与浓硫酸反应制备氯化氢,根据提供的仪器知,C装置用于固体与液体,加热制气体;(2)氯化镁晶体失去时发生水解,避免水解,在干燥氯化氢气体中加热氯化镁晶体,多余的氯化氢气体在吸附,避免污染环境,所以,仪器连接顺序为C A
A E
E B(3)A中装浓硫酸用于干燥,B中装氢氧化钠溶液用于吸收尾气;C中装氯化钠,D中装氯化镁晶体,F中装浓硫酸,用于制氯化氢(4)B装置吸收氯化氢,避免氯化氢排入空气中,污染环境(5)氯化氢极易溶于水,不能直接通入氢氧化钠溶液中,要防倒吸。
B(3)A中装浓硫酸用于干燥,B中装氢氧化钠溶液用于吸收尾气;C中装氯化钠,D中装氯化镁晶体,F中装浓硫酸,用于制氯化氢(4)B装置吸收氯化氢,避免氯化氢排入空气中,污染环境(5)氯化氢极易溶于水,不能直接通入氢氧化钠溶液中,要防倒吸。
 A
A E
E B(3)A中装浓硫酸用于干燥,B中装氢氧化钠溶液用于吸收尾气;C中装氯化钠,D中装氯化镁晶体,F中装浓硫酸,用于制氯化氢(4)B装置吸收氯化氢,避免氯化氢排入空气中,污染环境(5)氯化氢极易溶于水,不能直接通入氢氧化钠溶液中,要防倒吸。
B(3)A中装浓硫酸用于干燥,B中装氢氧化钠溶液用于吸收尾气;C中装氯化钠,D中装氯化镁晶体,F中装浓硫酸,用于制氯化氢(4)B装置吸收氯化氢,避免氯化氢排入空气中,污染环境(5)氯化氢极易溶于水,不能直接通入氢氧化钠溶液中,要防倒吸。
练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
 TiOCl2+2HCl↑)。在650~850℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。下图是实验室制备TiCl4的部分装置。
TiOCl2+2HCl↑)。在650~850℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。下图是实验室制备TiCl4的部分装置。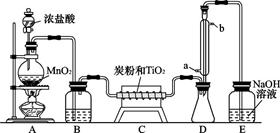
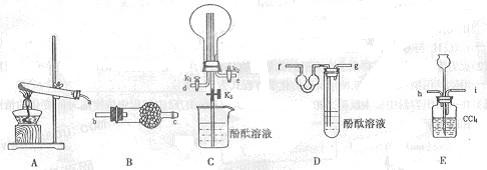
 ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(
ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(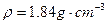 )110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
)110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质。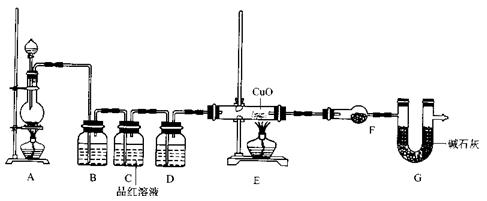
 + (CH3CO)2O
+ (CH3CO)2O 
 + CH3COOH
+ CH3COOH