籾朕坪否
厮岑(1) H2(g)⇦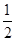 O2(g)﹆H2O(g) ◉ DH1﹆akJ,mol-1
O2(g)﹆H2O(g) ◉ DH1﹆akJ,mol-1
(2) 2H2(g)⇦O2(g)﹆2H2O(g) ◉ DH2﹆b kJ,mol-1
(3) H2(g)⇦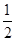 O2(g)﹆H2O(l)
◉ DH3﹆c kJ,mol-1
O2(g)﹆H2O(l)
◉ DH3﹆c kJ,mol-1
(4) 2H2(g)⇦O2(g)﹆2H2O(l) ◉ DH4﹆d kJ,mol-1
和双購狼塀嶄屎鳩議頁
A⤴ a〽c〽0 B⤴b﹅d﹅0 C⤴ 2a﹆b〽0 D⤴2c﹆d﹅0
‐基宛/
C
‐盾裂/
編籾蛍裂⦿狽賑伴付頁慧犯郡哘⇧夸@H弌噐0。歌紗郡哘議狽賑埆謹⇧慧竃議犯楚埆謹⇧夸2a﹆b〽0、2c﹆d〽0◉喇噐賑蓑邦議嬬楚互噐匣蓑議嬬楚⇧侭參狽賑伴付伏撹匣蓑邦扮慧犯謹⇧徽犯埆謹⇧@H埆弌⇧侭參屎鳩議購狼頁2c﹆d〽2a﹆b〽0⇧咀緩基宛僉C。
深泣⦿深臥郡哘犯寄弌曳熟

膳楼過狼双基宛
 A紗署籾 狼双基宛
A紗署籾 狼双基宛 畠單霞編壌狼双基宛
畠單霞編壌狼双基宛
屢購籾朕