题目内容
【题目】Z是一种常见的工业原料,实验室制备Z的化学方程式如下图所示。下列说法正确的是( )
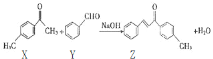
A.1molZ最多能与7molH2反应
B.Z分子中的所有原子一定共平面
C.可以用酸性KMnO4溶液鉴别X和Y
D.X的同分异构体中含有苯环和醛基的结构有14种(不考虑立体异构)
【答案】D
【解析】
A. 1分子Z中含有2个苯环、1个碳碳双键、1个羰基,则1molZ最多能与8molH2发生加成反应,故A错误;
B. Z分子中含有甲基,因此Z分子中的所有原子不可能共平面,故B错误;
C. X分子中苯环上含有侧键—CH3,Y分子中含有—CHO,则X和Y都能使酸性KMnO4溶液褪色,则不能用酸性KMnO4溶液鉴别X和Y,故C错误;
D. X的同分异构体中含有苯环和醛基的结构,取代基为—CH2CH2CHO的结构有1种,取代基为—CH(CHO)CH3的结构有1种,取代基为—CH2CH3和—CHO有3种,取代基为—CH2CHO和—CH3的结构有3种,取代基为2个—CH3和1个—CHO的结构有6种,共14种,故D正确。
综上所述,答案为D。

练习册系列答案
相关题目