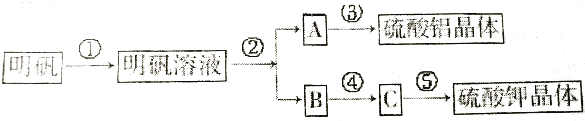
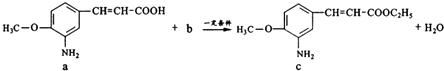题目内容
【题目】分别称取2.39 g (NH4)2SO4和NH4Cl固体混合物两份。
(1)将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]∶n(NH4Cl)为。
(2)另一份固体混合物中NH与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl)=(溶液体积变化忽略不计)。
【答案】
(1)1:2
(2)0.100mol·Lˉ1
【解析】解:n[(NH4)2SO4]=n(BaSO4)=0.01mol ,n(NH4Cl)=(2.39-0.01×132)/53.5=0.02mol
所以n[(NH4)2SO4]∶n(NH4Cl)=1:2 ;c[Ba(OH)2]=0.1mol/L ,2NH ~ Ba(OH)2 , ∵NH 总共0.04mol,∴n[Ba(OH)2]=0.02mol,∴加入V[Ba(OH)2]=0.02/0.1=0.2L,∴c(Cl—)=0.100mol/L。本题需要注意有效数字,有效数字不正确相应扣分。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目