题目内容
工业上测定SO2、N2、O2混合气体中SO2含量的装置如图。反应管中装有碘的淀粉溶液,SO2和I2发生反应为(N2、O2不与I2反应):SO2+I2+2H2O=H2SO4+2HI
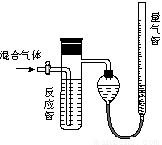
(1)混合气体进入反应管后,量气管内增加的水的体积等于_____________的体积(填写混合气体的分子式)
(2)读数前应冷却到室温、______________、___________
(3)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量_______(选填:偏高,偏低,不受影响)
(4)若碘溶液体积为Va mL,浓度为Cmol/L。N2与O2的体积为Vb mL(已折算成标准状况下的体积)。用C、Va、Vb表示SO2的体积百分含量为______________________。
(8分 每空2分)(1)N2、O2(2) 调整量器筒内外液面高度 平视凹液面读数
(3)偏低
(4)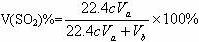
【解析】
试题分析:(1)由于N2、O2不与I2反应,所以混合气体进入反应管后,量气管内增加的水的体积等于N2、O2的体积。
(2)为了使读数准确,则必须使内外压强相等,则应该调整量器筒内外液面高度,另外读数时还要注意平视凹液面读数。
(3)反应管内溶液蓝色消失后,没有及时停止通气,则通过的气体总体积增加,所以测得的SO2含量偏低。
(4)根据方程式SO2+I2+2H2O=H2SO4+2HI可知,SO2的物质的量=0.001VaCmol,在标准状况下的体积是0.001VaCmol×22.4L/mol=0.0224VaCL=22.4VaCml,所以SO2的体积百分含量为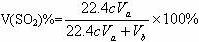 。
。
考点:考查工业尾气中SO2含量测定的实验探究
点评:该题是高考中的常见题型,属于中等难度的试题、试题基础性强,侧重对学生灵活运用基础知识解决实际问题的能力的培养,有利于培养学生规范严谨的实验设计能力。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。

(1)工业上用Na2SO3溶液处理工业尾气中的SO2,表中数据表示反应过程中
| n(SO32-) |
| n(HSO3-) |
|
91:9 | 1:1 | 9:91 | ||
| 室温下pH | 8.2 | 7.2 | 6.2 |
| n(SO32-) |
| n(HSO3-) |
(2)已知Ki1(H2SO3)>Ki(HAc)>Ki2(H2SO3)>Ki2(H2CO3),要使NaHSO3溶液中c(Na+):c(HSO3-)接近1:1,可在溶液中加入少量
a.H2SO3溶液 b.NaOH溶液 c.冰醋酸 d.Na2CO3
(3)实验室通过低温电解KHSO4溶液制备过二硫酸钾K2S2O8,写出熔融KHSO4的电离方程式:
(4)S2O82-有强氧化性,还原产物为SO42-,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液.书写此反应的化学方程式:
(5)已知:S2O32-有较强的还原性,实验室可用I-测定K2S2O8样品的纯度:反应方程式为:
S2O82-+2I-→2SO42-+I2 …①;
I2+2S2O32-→2I-+S4O62-…②.
则S2O82-、S4O62-、I2氧化性强弱顺序:
(6)K2S2O8是偏氟乙烯(CH2=CF2)聚合的引发剂,偏氟乙烯由CH3-CClF2气体脱去HCl制得,生成0.5mol偏氟乙烯气体要吸收54kJ的热,写出反应的热化学方程式
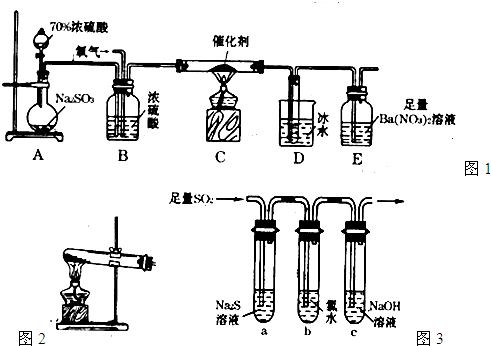
(12分)接触法制硫酸的主要原料是硫铁矿和空气。
I、接触法制硫酸的过程中,三个最主要的设备是: 、 和吸收塔;为了避免酸雾的形成,提高SO3的吸收率,工业上常用 来作吸收剂。
II、为了防止环境污染并对尾气进行综合利用,硫酸厂常用氨水吸收尾气中的SO2、SO3等气体,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。为了测定上述(NH4)2SO4 和NH4HSO4 固体混合物的组成,现称取该样品四份,分别加入浓度为3.00 mol·L-1的NaOH溶液50.00 mL,加热至120 ℃左右,使氨气全部逸出〔(NH4)2SO4和NH4HSO4的分解温度均高于200 ℃〕,测得有关实验数据如下(标准状况):
| 实验序号 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L |
| 1 | 3.62 | 50.00 | 0.896 |
| 2 | 7.24 | 50.00 | 1.792 |
| 3 | 10.86 | 50.00 | 2.016 |
| 4 | 14.48 | 50.00 | 1.568 |
为 L。
(2)14.48g该混合物中n((NH4)2SO4)= mol n(NH4HSO4)= mol
(3)第4组中过量的NH4+ 的物质的量为: mol
 ,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。
,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为 L。

