题目内容
【题目】已知H—H、H—O和OO键的键能分别为436 kJ·mol-1、463 kJ·mol-1和495 kJ·mol-1,下列热化学方程式正确的是( )
A. H2O(g)H2(g)+ ![]() O2(g) ΔH=-485 kJ·mol-1
O2(g) ΔH=-485 kJ·mol-1
B. H2O(g)H2(g)+ ![]() O2(g) ΔH=-242.5 kJ·mol-1
O2(g) ΔH=-242.5 kJ·mol-1
C. 2H2(g)+O2(g)2H2O(g) ΔH=+485 kJ·mol-1
D. 2H2(g)+O2(g)2H2O(g) ΔH=-485 kJ·mol-1
【答案】D
【解析】由题意,反应H2O(g)H2(g)+ ![]() O2(g)的ΔH=反应物总键能-生成物总键能=2×463 kJ·mol-1-436 kJ·mol-1-
O2(g)的ΔH=反应物总键能-生成物总键能=2×463 kJ·mol-1-436 kJ·mol-1-![]() ×495 kJ·mol-1=+242.5 kJ·mol-1,故A、B都错误;反应2H2(g)+O2(g)2H2O(g)的ΔH=反应物总键能-生成物总键能=2×436 kJ·mol-1+495 kJ·mol-1-2×2×463 kJ·mol-1=-485 kJ·mol-1,故C错误,D正确。
×495 kJ·mol-1=+242.5 kJ·mol-1,故A、B都错误;反应2H2(g)+O2(g)2H2O(g)的ΔH=反应物总键能-生成物总键能=2×436 kJ·mol-1+495 kJ·mol-1-2×2×463 kJ·mol-1=-485 kJ·mol-1,故C错误,D正确。

【题目】某化学小组研究盐酸被氧化的条件,进行如下实验。
(1)研究盐酸被MnO2氧化。
实验 | 操作 | 现象 |
Ⅰ | 常温下将MnO2和12mol/L浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
Ⅱ | 将I中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
Ⅲ | 加热MnO2和4mol/L稀盐酸混合物 | 无明显现象 |
① I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是________。
② Ⅱ中发生了分解反应,反应的化学方程式是________。
③ Ⅲ中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验IV进行探究:
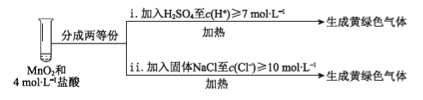
将实验Ⅲ、Ⅳ作对比,得出的结论是________;将实验现象Ⅳ中的ⅰ、ⅱ作对比,得出的结论是_______。
(2)研究盐酸能否被氧化性酸氧化。
① 烧瓶中放入浓H2SO4,通过分液漏斗向烧瓶中滴加浓盐酸,烧瓶上方立即产生白雾,用湿润的淀粉KI试纸检验,无明显现象。由此得出浓硫酸____(填“能”或“不能”)氧化盐酸。
② 向试管中加入3mL浓盐酸,再加入1mL浓HNO3,试管内液体逐渐变为橙色,加热,产生棕黄色气体,经检验含有NO2。
实验 | 操作 | 现象 |
Ⅰ | 将湿润的淀粉KI试纸伸入棕黄色气体中 | 试纸先变蓝,后褪色 |
Ⅱ | 将湿润的淀粉KI试纸伸入Cl2中 | 试纸先变蓝,后褪色 |
Ⅲ | …… | 试纸先变蓝,不褪色 |
通过实验I、Ⅱ、Ⅲ证明混合气体中含有Cl2,Ⅲ的操作是________。