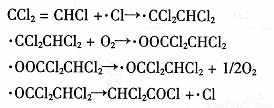题目内容
利用化学原理可以对工厂排放的废水进行有效检测与合理处理.
(1)染料工业排放的废水中含有大量有毒的NO2-,可以在碱性条件下加入铝粉除去(加热处理后的废水,会产生能使湿润的红色石蕊试纸变蓝的气体).除去NO2-的离子方程式为
________.(2)废水中的N、P元素是造成水体富营养化的关键因素,农药厂排放的废水中常含有较多的NH4+和PO43-,一般可以通过两种方法将其除去.
①方法一:将Ca(OH)2或CaO投加到待处理的废水中,生成磷酸钙,从而进行回收.当处理后的废水中c(Ca2+)=2×10-7 mol/L时,溶液中c(PO43-)=
________mol/L.(已知Ksp[Ca3(PO4)2]=2×10-33)②方法二:在废水中加入镁矿工业废水,就可以生成高品位的磷矿石―鸟粪石,反应的方程式为Mg2++NH4++PO43-=MgNH4PO4↓.该方法中需要控制污水的pH为7.5~10,若pH高于10.7,鸟粪石的产量会大大降低.其原因可能为
_____________.与方法一相比,方法二的优点为_______________.(3)三氯乙烯在印刷、纺织等行业应用广泛,为了减少其对环境的影响,可将三氯乙烯在二氧化钛薄膜上催化降解,其反应的机理如下:
●CCl2=CHCl+Cl→CCl2CHCl2
●CCl2CHCl2+O2→OOCCl2CHCl2
●
OOCCl2CHCl2→OCCl2CHCl2+1/2O2●OCCl2CHCl2→CHCl2COCl+Cl
该反应的总化学反应为
_____________.
答案:
解析:
解析:
|
(1)2Al+OH-+NO2-+2H2O=2AlO2-+NH3·H2O (2)①5×10-7 ②当pH高于10.7时,溶液中的Mg2+、NH4+会与OH-反应,平衡向逆反应方向移动 能同时除去废水中的氮,充分利用了镁矿工业废水 (3)2CCl2=CHCl+O2→2CHCl2COCl (每空2分,共10分) |

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目