题目内容
【题目】二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g)ΔH,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g)ΔH,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
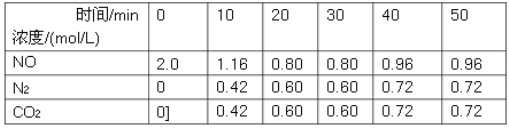
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率v(N2)=________mol/(Lmin);计算该反应的平衡常数K=___________。
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是________(填字母代号)。
A.加入合适的催化剂
B.适当缩小容器的体积
C.通入一定量的NO
D.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率________(填“升高”或“降低”),ΔH________0(填“>”或“<”).
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H1=-49.1kJ/mol
CH3OH(g)+H2O(g)△H1=-49.1kJ/mol
2CH3OH(g)![]() CH3OCH3(g)+H2O(g)△H2=-24.5kJ/mol
CH3OCH3(g)+H2O(g)△H2=-24.5kJ/mol
写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式__________________。
(3)二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池(电解质为KOH溶液)的负极反应式为:__________________
【答案】
(1)①0.03;0.56;②BC;③降低;<;
(2)CO2(g)+3H2(g) ![]() CH3OCH3(g)+3H2O(g) △H=-122.7 kJ/mol;
CH3OCH3(g)+3H2O(g) △H=-122.7 kJ/mol;
(3)CH3OCH3-12e-+16OH-=2CO32-+11H2O。
【解析】
试题分析:(1)①0~20min内,CO2的平均反应速率v(N2)=![]() =0.03molL-1min-1;C(s)+2NO(g)N2(g)+CO2(g),平衡浓度c(N2)=0.3mol/L;c(CO2)=0.3mol/L;c(NO)=0.4mol/L;反应的平衡常数K=
=0.03molL-1min-1;C(s)+2NO(g)N2(g)+CO2(g),平衡浓度c(N2)=0.3mol/L;c(CO2)=0.3mol/L;c(NO)=0.4mol/L;反应的平衡常数K=![]() =
=![]() =0.56;故答案为:0.03;0.56;
=0.56;故答案为:0.03;0.56;
②30min后,只改变某一条件,反应重新达到平衡,C(s)+2NO(g)N2(g)+CO2(g),依据图表数据分析,平衡状态物质浓度增大,依据平衡常数计算K=![]() =
=![]() =0.56,平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小溶液体积后加入一定量一氧化氮;A.加入合适的催化剂,催化剂只改变化学反应速率,不改变化学平衡,故A错误;B.适当缩小容器的体积,反应前后体积不变,平衡状态物质浓度增大,故B正确;C.通入一定量的NO,新平衡状态下物质平衡浓度增大,故C正确;D.加入一定量的活性炭,碳是固体对平衡无影响,平衡不动,故D错误;故答案为:BC;
=0.56,平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小溶液体积后加入一定量一氧化氮;A.加入合适的催化剂,催化剂只改变化学反应速率,不改变化学平衡,故A错误;B.适当缩小容器的体积,反应前后体积不变,平衡状态物质浓度增大,故B正确;C.通入一定量的NO,新平衡状态下物质平衡浓度增大,故C正确;D.加入一定量的活性炭,碳是固体对平衡无影响,平衡不动,故D错误;故答案为:BC;
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比从为5:3:3,氮气和二氧化碳难度之比始终为1:1,所以5:3>4:3,说明平衡向逆反应方向移动,达到新平衡时NO的转化率,说明逆反应是吸热反应,则正反应是放热反应;故答案为:降低;<;
(2)已知:①CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)△H1=-49.1kJ/mol,②2CH3OH(g)
CH3OH(g)+H2O(g)△H1=-49.1kJ/mol,②2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol,根据盖斯定律,将①×2+②得,CO2(g)+3H2(g)
CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol,根据盖斯定律,将①×2+②得,CO2(g)+3H2(g) ![]() CH3OCH3(g)+3H2O(g) △H=(-49.1kJ/mol)×2+(-24.5kJ/mol)=-122.7 kJ/mol,故答案为:CO2(g)+3H2(g)
CH3OCH3(g)+3H2O(g) △H=(-49.1kJ/mol)×2+(-24.5kJ/mol)=-122.7 kJ/mol,故答案为:CO2(g)+3H2(g) ![]() CH3
CH3
(3)二甲醚氧气电池(电解质为KOH溶液)中负极二甲醚失去电子生成碳酸根离子和水,电极反应式为CH3OCH3-12e-+16OH-=2CO32-+11H2O,故答案为:CH3OCH3-12e-+16OH-=2CO32-+11H2O。