题目内容
(1)最近有人利用反应“2C4H10+13O2=8CO2+10H2O”制造了一种燃料电池,一个电极通入空气,另一电极通入丁烷,电池的电解质是掺杂了Y2O3(三氧化 二钇)的ZrO2(二氧化
二钇)的ZrO2(二氧化 锆)晶体,它在高温下能传导O2-。试回答下列问题:
锆)晶体,它在高温下能传导O2-。试回答下列问题:
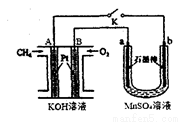
固体电解质中的O2-向 极移动(填“正”或“负”);写出该燃料电池的电极反应式:电池正极 ;电池负极 。
(2)用如图装置电解MnSO4溶液制MnO2时,A极为: 极, A电极电极反应式为 ;a极为: 极,电解MnSO4溶液制MnO2的化学方程式 。电解一段时间后, 溶液的pH将 (填“增大”、“减小”或“不变”)。
(3)精炼铜时,粗铜应与直流电源的____________极(填“正”或“负”)相连,阴极的电极反应式为 。
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案分卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于元素周期表的__________区;溴原子基态的价电子排布式为____________。
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是__________。
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是__________(写出名称)。
| 氟 | 氯 | 溴 | 碘 |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(4)已知ClO2-为角型,中心氯原子周围有四对价层电子。ClO2-中心氯原子的杂化轨道类型为____________,写出一个ClO2-的等电子体__________。
(5)下图为碘晶体晶胞结构。有关说法中正确的是_________。
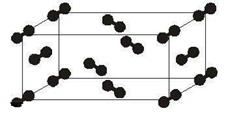
碘晶体晶胞
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子交替形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(6)已知CaF2晶体(见下图)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为___________。

某同学将光亮镁条放入盛有NH4Cl溶液的试管中,有大量气泡产生。为探究该反应原理,该同学做了以下试验并观察到相关现象,由此得出的结论不合理的是 ( ):
选项 | 实验及现象 | 结论 |
A | 将润湿红色石蕊试纸靠近试管口,试纸变蓝 | 反应中有NH3产生 |
B | 收集产生的气体并点燃,火焰呈淡蓝色 | 反应中有H2产 |
C | 收集气体的同时测得溶液的pH为8.0 | 生成Mg (OH)2 |
D | 向NH4Cl溶液中加锌,也有大量气泡产生 | 活泼金属可促进NH4+水解 |



 = 。
= 。
 程度不相同
程度不相同
 生
生 使溶液呈弱碱性
使溶液呈弱碱性