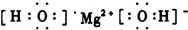题目内容
A、B、C、D均为短周期元素。A、B可形成两种液态化合物,其实验式分别为BA和B(1)写出元素的名称:A____________,C____________。
(2)Y分子是____________分子(填“极性”或“非极性”)。
(3)写出实现下列转化的化学反应方程式并标明电子转移的方向和数目:
C2+(BA)n![]() A2___________________________________________
A2___________________________________________
(4)B
(1)氧 氯
(2)极性
![]()
(4)![]() +H2O
+H2O![]() NH3·H2O+H+
NH3·H2O+H+
解析:此题考查了元素周期表、元素化合物的知识。据题意,A、B、C、D四种元素,由A、B可形成两种液态化合物,其实验式分别为BA和B

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
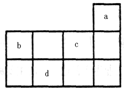 a、b、c、d均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )
a、b、c、d均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )| A、a原子的最外电子层上有8个电子 | B、c的最高价氧化物对应水化物为强酸 | C、d的原子半径比c的大 | D、b的非金属性比c的强 |


 A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素:A、B、C三种元素的原子序数之和为31;D元素与A、B、C三种元素既不是同周期,也不同主族.请回答:
A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素:A、B、C三种元素的原子序数之和为31;D元素与A、B、C三种元素既不是同周期,也不同主族.请回答:
 NH3?H2O+H+
NH3?H2O+H+ 2NH3
2NH3