题目内容
(18分)高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿(主要成份MnO2)制备高锰酸钾的流程图。

(1)软锰矿粉碎的目的 。
软锰矿、KOH混合物在空气加热熔融反应生成K2MnO4的化学方程式为:
。操作Ⅲ的名称为 。
(2)反应②的化学方程式为 。
以上生产流程中可循环利用的物质是Ca(OH)2、CO2、 、 。
工业上用上述原理生产KMnO4方法产率较低,较好的制备方法是电解法。用Pt作阳极,Fe作阴极,电解K2MnO4溶液,阳极的电极反应式为 。
(3)KMnO4是一种较稳定的化合物,但日光对KMnO4溶液的分解有催化作用,生成MnO2、KOH和O2。而MnO2也是该分解反应的一种催化剂,请你设计一个实验方案,验证MnO2对该分解反应具有催化性。简述实验操作、现象及相关结论:
。

(1)软锰矿粉碎的目的 。
软锰矿、KOH混合物在空气加热熔融反应生成K2MnO4的化学方程式为:
。操作Ⅲ的名称为 。
(2)反应②的化学方程式为 。
以上生产流程中可循环利用的物质是Ca(OH)2、CO2、 、 。
工业上用上述原理生产KMnO4方法产率较低,较好的制备方法是电解法。用Pt作阳极,Fe作阴极,电解K2MnO4溶液,阳极的电极反应式为 。
(3)KMnO4是一种较稳定的化合物,但日光对KMnO4溶液的分解有催化作用,生成MnO2、KOH和O2。而MnO2也是该分解反应的一种催化剂,请你设计一个实验方案,验证MnO2对该分解反应具有催化性。简述实验操作、现象及相关结论:
。
(18分)
(1)增大反应物接触面积,加快反应速率,使反应物反应完全(3分)2 MnO2+O2+4KOH=
2K2MnO4+2H2O (3分) 重结晶(2分)
(2)3K2MnO4 +2 CO2 =2KMnO4 +2K2CO 3 +MnO2↓(3分) KOH、MnO2(2分)
MnO42— -e —= MnO4—(2分)
(3)取两份等体积、等浓度的KMnO4溶液,在同样条件下,只在其中一份中加入少量MnO2,观察溶液紫红色褪去的快慢。(其他合理答案也可)(3分)
(1)增大反应物接触面积,加快反应速率,使反应物反应完全(3分)2 MnO2+O2+4KOH=
2K2MnO4+2H2O (3分) 重结晶(2分)
(2)3K2MnO4 +2 CO2 =2KMnO4 +2K2CO 3 +MnO2↓(3分) KOH、MnO2(2分)
MnO42— -e —= MnO4—(2分)
(3)取两份等体积、等浓度的KMnO4溶液,在同样条件下,只在其中一份中加入少量MnO2,观察溶液紫红色褪去的快慢。(其他合理答案也可)(3分)
略

练习册系列答案
相关题目
 +4)制取纳米级TiO2的流程如下:
+4)制取纳米级TiO2的流程如下: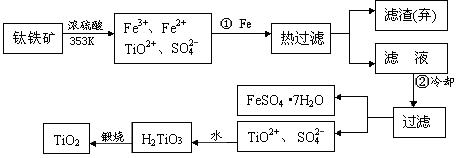
 TiCl4
TiCl4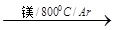 Ti
Ti 
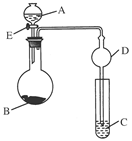
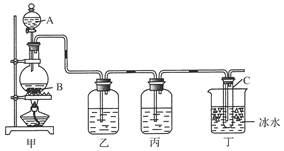

 G H I
G H I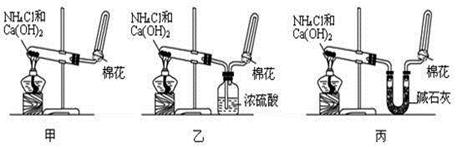
 )检验氨气是否收集满的方法是(简述操作方法、现象和结
)检验氨气是否收集满的方法是(简述操作方法、现象和结 论)____________________
论)____________________ 用NH4Cl固体代替制NH3?______________(填“能”或“不能”)。
用NH4Cl固体代替制NH3?______________(填“能”或“不能”)。
 制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:将 ,
制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:将 , (填“大”或“小”),有 气味。
(填“大”或“小”),有 气味。