题目内容
【题目】现进行实验,测定草酸晶体(H2C2O4·xH2O)中的x值;
(1)称取Wg草酸晶体,配成100.00mL溶液
(2)取25.00mL所配溶液于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定至KMnO4不再褪色为止,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
①本实验中,必需要用的仪器有(从下列仪器中选择,填序号)__________________,还缺少的仪器有(填名称):_______________________。
A、托盘天平(带砝码、镊子)
B、滴定管
C、100mL的量筒
D、100mL的容量瓶
E、烧杯
F、漏斗
G、锥形瓶
H、玻璃棒
I、药匙
J、烧瓶
②标准液KMnO4溶液应装在__________式滴定管中。
③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得的x的值会__________(填偏大、偏小、无影响)。
④在滴定过程中若用去amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为_________mol·L-1,由此,x=__________。
⑤若滴定终点读数时仰视刻度,则计算的x值会__________(填偏大、偏小、无影响)。
【答案】①ABDEGHI 胶头滴管、铁架台带滴定管夹②酸 ③无影响
④0.1av mol·L-1;x=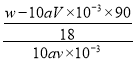 或
或![]() -5 ⑤偏小
-5 ⑤偏小
【解析】
试题分析:①实验中为了配制准确浓度的草酸溶液以及进行氧化还原滴定,所需要的实验仪器主要有天平(含砝码)、烧杯、药匙、100mL容量瓶、胶头滴管、玻璃棒、滴定管、锥形瓶等,故还需要胶头滴管、 铁架台带滴定管夹;
②KMnO4溶液具有强氧化性,可以腐蚀橡皮管,故KMnO4溶液应装在酸式滴定管中;
③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,溶质的物质的量不变,则所测得的x的值不受影响;
④滴定中消耗KMnO4溶液体积为VmL,n(KMnO4)=a molL﹣1×V×10﹣3L=0.001aVmol,根据关系式2KMnO4~5H2C2O4可知25.0mL草酸溶液中n(H2C2O4)=2.5×0.001aVmol,所以100mL草酸溶液中n(H2C2O4)=2.5×0.001aVmol×4=0.01aVmol,因此草酸的浓度为 0.01aVmol ÷0.1L=0.1av mol·L-1;草酸晶体中草酸的质量为0.01aVmol×90g/mol,由化学式可知x=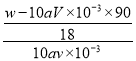 或
或![]() -5。
-5。
⑤读取终点读数时仰视,读数偏大,导致KMnO4溶液体积偏小,计算测定的草酸的质量偏大,故x的值偏小。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案