题目内容
【题目】0.1 mol某金属单质与足量的盐酸反应,放出1.12LH2(标准状况),并转变为具有Ar原子的电子层结构的离子,该金属元素在元素周期表中的位置是
A.第三周期第IA族 B.第四周期第IA族
C.第三周期第ⅡA族 D.第四周期第ⅡA族
【答案】B
【解析】
试题0.1 mol某金属单质与足量的盐酸反应,放出1.12LH2(标准状况),其中氢气的物质的量是1.12L÷22.4L/mol=0.05mol,这说明0.1mol均是失去0.1mol电子,则金属是第IA族元素。由于能转变为具有Ar原子的电子层结构的离子,则该金属是K,位于第四周期第IA族,答案选B。

练习册系列答案
相关题目
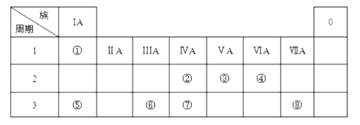
【题目】下表是周期表中的一部分,根据A﹣I在周期表中的位置,第(1)~(4)小题用元素符号或化学式回答,(5)~(6)小题按题目要求回答.
族 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
1 | A | |||||||
2 | D | E | G | I | ||||
3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是 , 只有负价而无正价的是 , 氧化性最强的单质是 , 还原性最强的单质是 .
(2)最高价氧化物的水化物中碱性最强的是 , 酸性最强的是 , 呈两性的是 .
(3)A分别与D,E,F,G,H形成的化合物中,最稳定的
(4)在B,C,E,F,G,H中,原子半径最大的是
(5)A和D组成化合物的电子式
(6)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式 .