题目内容
【题目】某混合物的水溶液中,只可能含有以下离子中的若干种:K+、Mg2+、Fe3+、Al3+、NH4+、Cl﹣、CO32﹣和SO42﹣ . 现每次取10.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体0.672L(标准状况下),但整个过程中无沉淀生成.
③第三份加入足量BaCl2溶液后得干燥沉淀6.63g,沉淀经足量盐酸洗涤,干燥后剩余4.66g.
请回答:
(1)c(CO32﹣)=mol/L.
(2)K+是否存在?(填“存在”或“不存在”);若存在,浓度范围是(若不存在,则不必回答第2问).
(3)根据以上实验,不能判断哪种离子是否存在? , 若存在,这种离子如何进行检验? .
【答案】
(1)1
(2)存在,c(K+)≥3mol/L
(3)Cl﹣,取少量溶液于试管中,滴加过量Ba(NO3)2溶液后,取上层清夜,再滴加AgNO3溶液,若有白色沉淀,则证明有Cl﹣
【解析】解:(1)根据实验③现象,酸洗涤沉淀前后,质量减少,减少的质量为碳酸钡的质量,
Ba2++ | CO32﹣= | BaCO3↓ |
1mol | 197g | |
n(CO32﹣) | (6.63﹣4.66)g=1.97g |
则n(CO32﹣)= ![]() =0.01mol
=0.01mol
碳酸根的物质的量浓度为:c(CO32﹣)= ![]() =1mol/L
=1mol/L
(2)根据实验③现象,酸洗涤沉淀后沉淀的质量为硫酸钡的质量,
Ba2++ | SO42﹣= | BaSO4↓ |
1mol | 233g | |
0.02mol | 4.66g |
铵根离子的物质的量为
NH4++OH﹣ | NH3↑+H2O |
1mol | 22.4L |
0.03mol | 0.672L |
根据溶液中阴阳离子所带电荷相等得,钾离子存在;一个硫酸根离子、一个碳酸根离子都各带两个单位的负电荷,一个铵根离子、一个钾离子各带一个单位的正电荷,
设其物质的量为xmol,根据溶液中阴阳离子所带电荷相等列方程式:0.01mol×2+0.02mol×2=0.03m0l×1+xmol×1,
解得:x=0.03,
由于溶液中可能存在氯离子,则钾离子的浓度满足:c(K+)≥ ![]() =3mol/L;
=3mol/L;
(3)根据实验①现象判断,不能判断氯离子是否存在;氯离子和银离子反应生成白色沉淀,且该沉淀不溶于水和硝酸,所以可用硝酸酸化的硝酸银溶液检验,但先判断硫酸根离子的干扰
所以答案是:(1)1; (2)存在;c(K+)≥3mol/L;(3)Cl﹣;取少量溶液于试管中,滴加过量Ba(NO3)2溶液后,取上层清夜,再滴加AgNO3溶液,若有白色沉淀,则证明有Cl﹣。

【题目】已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH,HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
CH3COOH | HClO | H2CO3 |
Ka=1.8×10﹣5 | Ka=3.0×10﹣8 | Ka1=4.4×10﹣7 Ka2=4.7×10﹣11 |
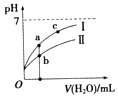
A.如图中的两种酸分别和等浓度的NaOH溶液刚好完全反应,消耗碱的体积相等
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO﹣+CO2+H2O═2HClO+CO32﹣
C.a、b、c三点所示溶液中水的电离程度c>a>b
D.图象中,Ⅰ表示CH3COOH,Ⅱ表示HClO,且溶液导电性:c>b>a