题目内容
 试回答下列问题:
试回答下列问题:
(1)漂粉精在空气中长期露置时会变质,则其变质的有关化学方程式为______.
(2)把1molNa和1mol Mg分别投入到过量且等体积的盐酸中,分别得到溶液a和b,则溶液a和b的质量关系为ma______mb
(3)如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试根据标签上的有关数据回答下列问题:
①该浓盐酸中HCl的物质的量浓度为______mol/L.
②标准状况下,1.00L水(密度:1.00g?cm-3)吸收______L的HCl可制得上述浓盐酸.
解:(1)因碳酸的酸性大于次氯酸,故漂粉精中的Ca(ClO)2与二氧化碳反应发生反应:
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,符合强酸制弱酸.
故答案为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
(2)0.1mol的Mg为2.4g,置换出0.1mol氢气即0.2g的氢气,差量为2.4g-0.2g=2.2g,即溶液增重2.2g;0.1mol的Na为2.3g,置换出0.05mol氢气即0.1g的氢气,差量为2.3g-0.1g=2.2g,即溶液增重2.2g,而原来盐酸的质量相等,所以反应后两溶液的质量相等.
故答案为:等于
(3)①设盐酸的体积为VL,则溶质的质量为V×1000mL×1.19g?cm-3×36.5%,溶质的物质的量为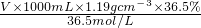 =11.9Vmol,所以溶质的物质的量浓度为
=11.9Vmol,所以溶质的物质的量浓度为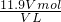 =11.9mol/L.
=11.9mol/L.
②1.00L水(密度:1.00g?cm-3)的质量为1000g,设HCl气体的体积为VL,则
W= ×100%=
×100%=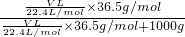 ×100%=36.5%,解得V=353
×100%=36.5%,解得V=353
故答案为:353
分析:(1)根据漂粉精与二氧化碳反应书写化学方程式;
(2)根据差量法求出盐酸增重的质量,判断反应后溶液的质量;
(3)①设溶液的体积为VL,再求出溶质的物质的量,代入公式求出物质的量浓度;
②先求出水的质量,设HCl气体的体积为VL,根据质量百分数等于溶质的质量除以溶液的质量,求出溶质的体积;
点评:本题考查了盐酸的性质以及根据溶质质量分数求出物质的量浓度,利用溶质质量分数求出溶质的质量和体积.
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,符合强酸制弱酸.
故答案为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
(2)0.1mol的Mg为2.4g,置换出0.1mol氢气即0.2g的氢气,差量为2.4g-0.2g=2.2g,即溶液增重2.2g;0.1mol的Na为2.3g,置换出0.05mol氢气即0.1g的氢气,差量为2.3g-0.1g=2.2g,即溶液增重2.2g,而原来盐酸的质量相等,所以反应后两溶液的质量相等.
故答案为:等于
(3)①设盐酸的体积为VL,则溶质的质量为V×1000mL×1.19g?cm-3×36.5%,溶质的物质的量为
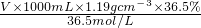 =11.9Vmol,所以溶质的物质的量浓度为
=11.9Vmol,所以溶质的物质的量浓度为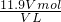 =11.9mol/L.
=11.9mol/L.②1.00L水(密度:1.00g?cm-3)的质量为1000g,设HCl气体的体积为VL,则
W=
 ×100%=
×100%=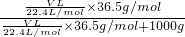 ×100%=36.5%,解得V=353
×100%=36.5%,解得V=353故答案为:353
分析:(1)根据漂粉精与二氧化碳反应书写化学方程式;
(2)根据差量法求出盐酸增重的质量,判断反应后溶液的质量;
(3)①设溶液的体积为VL,再求出溶质的物质的量,代入公式求出物质的量浓度;
②先求出水的质量,设HCl气体的体积为VL,根据质量百分数等于溶质的质量除以溶液的质量,求出溶质的体积;
点评:本题考查了盐酸的性质以及根据溶质质量分数求出物质的量浓度,利用溶质质量分数求出溶质的质量和体积.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目



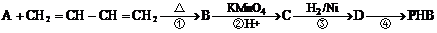
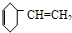
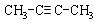
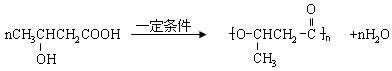
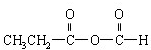
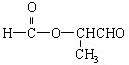
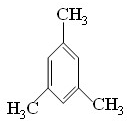 、
、


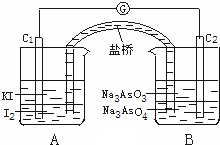 已知可逆反应:AsO43-+2I-+2H+?AsO33-+I2+H2O据此设计出如图所示的实验装置(装置中盐桥的作用是使整个装置形成一个闭合回路).进行如下操作:
已知可逆反应:AsO43-+2I-+2H+?AsO33-+I2+H2O据此设计出如图所示的实验装置(装置中盐桥的作用是使整个装置形成一个闭合回路).进行如下操作: