题目内容
下列有关实验装置进行的相应实验,能达到实验目的的是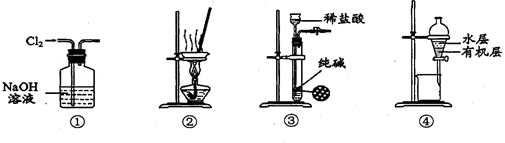
| A.用装置①除去Cl2中含有的少量HCl |
| B.用装置②从氯化铁溶液中直接蒸发结晶获得无水氯化铁 |
| C.用装置③制取少量纯净的CO2气体 |
| D.用装置④分离CCl4萃取碘水后已分层的有机层和水层 |
D
解析试题分析:洗气瓶中的氢氧化钠溶液不仅能与氯化氢反应,而且能与氯气反应,因此不能达到实验目的,应选择饱和食盐水除去氯气中含有的氯化氢,故A错误;氯化铁是强酸弱碱盐,蒸发溶液导致其彻底发生水解反应,生成氢氧化铁沉淀和氯化氢气体,氢氧化铁受热会分解生成氧化铁和水,因此最终产物是氧化铁固体,没有无水氯化铁,故B错误;纯碱的化学式是Na2CO3,稀盐酸的酸性比碳酸强,与纯碱能反应放出二氧化碳气体,但是稀盐酸能挥发出氯化氢气体和水蒸气,因此制取的二氧化碳中混有少量的氯化氢和水,故C错误;四氯化碳与水互不相溶,密度比水重,因此出现分层现象,四氯化碳位于下层,水位于上层,故D正确。
考点:考查化学实验方案的设计与评价,设计除去氯气中混有的氯化氢、氯化铁的水解反应、二氧化碳的制取、分液等。

练习册系列答案
相关题目
要除去FeCl3溶液中的少量FeCl2杂质,可向其中加入适量的
| A.Fe | B.氯水 | C.盐酸 | D.NaOH溶液 |
下列说法正确的是
| A.用盐析法分离NaCl溶液和淀粉胶体 |
| B.除去苯中少量苯酚,向混合物中加人足量的NaOH溶液后过滤 |
| C.加足量的稀盐酸可除去BaCO3固体中少量的BaSO4 |
| D.向硝酸银稀溶液中逐滴加人稀氨水至白色沉淀恰好溶解,即得银氨溶液 |
下列属于分离、提纯固态有机物的操作的是
| A.蒸馏 | B.萃取 | C.分液 | D.重结晶 |
下列混合物能用分液法分离的是 ( )
| A.乙醇与乙酸 | B.苯和溴苯 |
| C.乙酸乙酯和Na2CO3溶液 | D.葡萄糖与果糖混合液 |
下列叙述不正确的是( )
| A.可以用溴水来鉴别乙烯和苯 |
| B.可以用金属钠来鉴别乙醇和乙酸 |
| C.可以用新制的氢氧化铜来鉴别葡萄糖和淀粉 |
| D.可以用灼烧的方法来鉴别真丝布料和纯棉布料 |
工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),并用来生产Zn(NO3)2·6H2O晶体,其工艺流程为:
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 5.4 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.0 |
⑴在“酸浸”步骤中,为提高锌的浸出速率,除通入空气“搅拌”外,还可采取的措施是 。
⑵上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有 。
⑶在“除杂I”步骤中,需再加入适量H2O2溶液,H2O2与Fe2+反应的离子方程式为 。为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为 。检验Fe3+是否沉淀完全的实验操作是 。
⑷加入Zn粉的作用是 。“操作A”的名称是 。

