题目内容
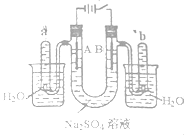
【题目】下列金属防腐的措施中,使用外加电流的阴极保护法的是( )
A. 水中钢闸门连接电源的负极 B. 金属护栏表面涂漆
C. 汽水底盘喷涂高分子膜 D. 地下管道连接镁块
【答案】A
【解析】试题分析:A.水中的钢闸门连接电源负极,阴极上得电子被保护,所以属于使用外加电流的阴极保护法,故A正确;B.对健身器材涂油漆使金属和空气、水等物质隔离而防止生锈,没有连接外加电源,故B错误;C.汽车底盘喷涂高分子膜阻止了铁与空气、水的接触,从而防止金属铁防锈,没有连接外加电源,故C错误;D.镁的活泼性大于铁,用牺牲镁块块的方法来保护船身而防止铁被腐蚀,属于牺牲阳极的阴极保护法,故D错误;故选A。

【题目】已知反应H2(g)+ I2(g)![]() 2HI(g),1 mol H2完全反应放出a kJ的热量,依据下表数据,以下说法错误的是( )
2HI(g),1 mol H2完全反应放出a kJ的热量,依据下表数据,以下说法错误的是( )
化 学 键 | H—H | I—I |
断开1 mol化学键时吸收的能量(kJ) | b | c |
A.该反应中反应物的总能量高于生成物的总能量
B.断开1 mol H-H 键和1 mol I-I 键所需能量大于断开2 mol H-I 键所需能量
C.断开2 mol H-I键所需能量为(a+b+c)kJ
D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
【题目】某温度时,在2 L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:
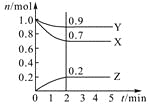
(1)该反应的化学方程式为 。
(2)反应开始至2 min,用Y表示的平均反应速率为 ,X的转化率为 。
(3)在一定温度下,下列情况可作为上述反应达到反应限度的标志的是 。
A.X、Y、Z的浓度相等 |
B.X、Y、Z的分子数比为3︰1︰2 |
C.Z的生成速率是Y的生成速率的二倍 |
D.单位时间内生成n mol Y,同时生成3n mol X |
(4)在密闭容器里,通入a mol A(g)和b mol B(g),
发生反应A(g)+ B(g)= 2C(g),当改变下列条件时,会加快反应速率的是 (填序号)。
①降低温度
②保持容器的体积不变,充入氦气
③加入催化剂
④保持容器的体积不变,增加A(g)的物质的量