题目内容
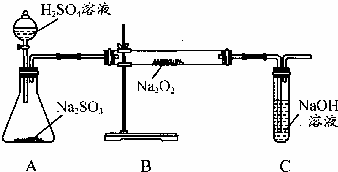 某化学学习小组的同学为探究过氧化钠与二氧化硫的反应,用如图所示的装置进行实验.通入足量的气体后将带火星的木条插入试管C中木条复燃.请回答下列问题
某化学学习小组的同学为探究过氧化钠与二氧化硫的反应,用如图所示的装置进行实验.通入足量的气体后将带火星的木条插入试管C中木条复燃.请回答下列问题(1)A中发生的反应方程式为
(2)该化学学习小组的同学对B中的反应给予下列两种猜想:
①第1小组同学认为Na2O2与SO2反应类似Na2O2与CO2间的反应,据此分析反应后B中白色固体物质为
②第2小组同学认为B中还有其他反应发生,并产生支持燃烧的气体,该反应的化学方程式是
(3)有资料显示SO2在一定条件下可以被Na2O2氧化为Na2SO4.请设计实验以检验B中白色固体是否含有Na2SO4
分析:(1)装置图分析可知装置A中是二氧化硫气体的发生装置,制备二氧化硫用75%的浓硫酸减少二氧化硫气体的溶解;
(2)①Na2O2与SO2反应类似Na2O2与CO2间的反应,判断生成产物为高价态的硫酸钠;
②二氧化氯气体中含有水蒸气,和过氧化钠反应生成氧气;为完成探究过氧化钠与二氧化硫的反应还必需对上述装置进行改进,除去水蒸气;
(3)依据硫酸根离子的检验方法设计实验验证;
(2)①Na2O2与SO2反应类似Na2O2与CO2间的反应,判断生成产物为高价态的硫酸钠;
②二氧化氯气体中含有水蒸气,和过氧化钠反应生成氧气;为完成探究过氧化钠与二氧化硫的反应还必需对上述装置进行改进,除去水蒸气;
(3)依据硫酸根离子的检验方法设计实验验证;
解答:解:(1)装置图分析可知装置A中是二氧化硫气体的发生装置,反应的化学方程式为:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;二氧化硫易溶于水,制备二氧化硫用75%的浓硫酸减少二氧化硫气体的溶解;
故答案为:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;减小二氧化硫的溶解.
(2)①第1小组同学认为Na2O2与SO2反应类似Na2O2与CO2间的反应,据此分析反应后B中白色固体物质为六元素高价态的盐为Na2SO4;
故答案为:Na2SO4;
②二氧化氯气体中含有水蒸气,和过氧化钠反应生成氧气,反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为完成探究过氧化钠与二氧化硫的反应还必需对上述装置进行改进,除去水蒸气,气体在通入B装置之前加一个干燥二氧化硫的装置;
故答案为:2Na2O2+2H2O=4NaOH+O2↑;气体在通入B装置之前加一个干燥二氧化硫的装置;
(3)验B中白色固体是否含有Na2SO4,依据硫酸根离子的检验方法设计实验验证,取反应后的适量白色固体溶于水,然后加入足量的盐酸溶液,最后在加入足量的BaCl2溶液,若有白色沉淀产生,即说明Na2SO4含有;
故答案为:取反应后的适量白色固体溶于水,然后加入足量的盐酸溶液,最后在加入足量的BaCl2溶液,若有白色沉淀产生,即说明Na2SO4含有.
故答案为:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;减小二氧化硫的溶解.
(2)①第1小组同学认为Na2O2与SO2反应类似Na2O2与CO2间的反应,据此分析反应后B中白色固体物质为六元素高价态的盐为Na2SO4;
故答案为:Na2SO4;
②二氧化氯气体中含有水蒸气,和过氧化钠反应生成氧气,反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;为完成探究过氧化钠与二氧化硫的反应还必需对上述装置进行改进,除去水蒸气,气体在通入B装置之前加一个干燥二氧化硫的装置;
故答案为:2Na2O2+2H2O=4NaOH+O2↑;气体在通入B装置之前加一个干燥二氧化硫的装置;
(3)验B中白色固体是否含有Na2SO4,依据硫酸根离子的检验方法设计实验验证,取反应后的适量白色固体溶于水,然后加入足量的盐酸溶液,最后在加入足量的BaCl2溶液,若有白色沉淀产生,即说明Na2SO4含有;
故答案为:取反应后的适量白色固体溶于水,然后加入足量的盐酸溶液,最后在加入足量的BaCl2溶液,若有白色沉淀产生,即说明Na2SO4含有.
点评:本题考查了物质性质的实验探究方法和应用,主要是过氧化钠性质,硫酸根离子检验,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
 乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4?xH2O)中x值.通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4?xH2O)中x值.通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定: 某化学学习小组的同学欲探究测定草酸晶体(H2C2O4?xH2O)中x的值.通过查阅资料该小组同学得知:草酸易溶于水,其水溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.该组同学利用该反应原理设计了滴定的方法测定x值.
某化学学习小组的同学欲探究测定草酸晶体(H2C2O4?xH2O)中x的值.通过查阅资料该小组同学得知:草酸易溶于水,其水溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.该组同学利用该反应原理设计了滴定的方法测定x值.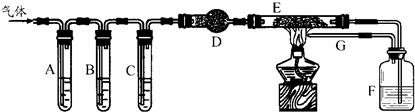
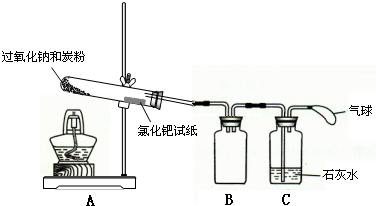 钠的化合物都有广泛的应用,其中Na2O2就是一种常见的氧化剂.某化学学习小组的同学欲通过以下实验探究炭粉与Na2O2反应的产物.
钠的化合物都有广泛的应用,其中Na2O2就是一种常见的氧化剂.某化学学习小组的同学欲通过以下实验探究炭粉与Na2O2反应的产物.