题目内容
3.工业上常利用“隔膜电解法”处理高浓度乙醛废水.其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O═CH3CH2OH+CH3COOH.实验室按如图所示装置来模拟乙醛废水的处理(以一定浓度的乙醛和Na2SO4溶液为电解质溶液).①若以甲醇碱性燃料电池为直流电源,则燃料电池中b极应通入CH3OH(填化学式).

②电解池阳极区的电极反应式为CH3CHO-2e-+H2O=CH3COOH+2H+.
③在实际工艺处理中,阴极区乙醛的去除率可达60%.若在两极区分别注入乙醛含量为3g•L-1的废水1m3,可得到乙醇1.88kg(计算结果保留小数点后两位).
分析 ①连接电解池阴极的是原电池负极,燃料电池负极上投放燃料,燃料失电子发生氧化反应;
②阳极上乙醛失电子发生氧化反应生成乙酸;
③先根据废水的质量、乙醛的去除率计算去除乙醛的质量,再根据乙醛和乙醇的关系式计算生成乙醇的质量.
解答 解:①连接电解池阴极的是原电池负极,负极上燃料失电子发生氧化反应,该燃料电池中燃料是甲醇,所以b电极上投放的是CH3OH,故答案为:CH3OH;
②电解过程中,阳极上失电子发生氧化反应,阴极上得电子发生还原反应,所以阳极上乙醛和氢氧根离子放电,所以除了氢氧根离子失电子外,乙醛失电子发生氧化反应,电极反应式为CH3CHO-2e-+H2O=CH3COOH+2H+;
故答案为:CH3CHO-2e-+H2O=CH3COOH+2H+;
③设生成乙醇的质量是x,
废水中乙醛的质量为1m3×3g/L=3kg,乙醛的去除率为60%,则反应的乙醛为1.8kg,
CH3CHO+2e-+2H2O═CH3CH2OH+2OH-
44 46
1.8kg x
x=1.88kg,
故答案为:1.88.
点评 本题在电化学的基础上综合考查原电池和电解池的反应原理等知识,题目较为综合,难度中等,注意燃料电池电极反应式的书写要结合电解质溶液.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列关于实验现象的描述不正确的是( )
| A. | 铜锌组成的原电池中电子是从锌经过导线流向铜 | |
| B. | 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 | |
| C. | 把铜片插入FeCl3溶液中,在铜片表面出现一层铁 | |
| D. | 把锌片放入盛有盐酸的试管中,加入几滴CuCl2溶液,气泡放出速率加快 |
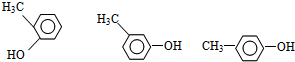
14.已知:乙醇可被强氧化剂氧化为乙酸. 可经三步反应制取
可经三步反应制取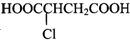 ,第二步的反应类型是( )
,第二步的反应类型是( )
 可经三步反应制取
可经三步反应制取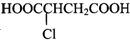 ,第二步的反应类型是( )
,第二步的反应类型是( )| A. | 水解反应 | B. | 加成反应 | C. | 氧化反应 | D. | 消去反应 |
11.依据元素周期表及元素周期律,下列推断正确的是( )
| A. | H2SO4的酸性比H2CO3的强 | B. | Mg(OH)2的碱性比Ca(OH)2的弱 | ||
| C. | HCl、HBr、HI的热稳定性依次增强 | D. | 氯气比氟气更易与氢气发生反应 |
18.下列说法中,正确的是( )
| A. | 0.l mol•L-1醋酸钙溶液中,c(Ca2+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 等体积等pH的NH4Cl溶液、盐酸,完全溶解少量且等同的锌粉,前者用时少 | |
| C. | 将n mol H2(g)、n mol I2(g)和2n mol H2 (g)、2n mol I2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者 | |
| D. | 某物质的溶液中由水电离出的c(H+)=1×10-a mol•L-1,若a>7时,则该溶液的pH一定为14-a |
15.下列说法正确的是( )
| A. | 分子组成上相差1个或若干个CH2原子团的有机物互为同系物 | |
| B. | 凡是分子组成相同而结构不同的有机物之间互为同分异构体 | |
| C. | 苯分子中不存在C-C和C=C的事实是分子中六个碳碳键的键长、键角、键能都相等,邻二氯苯没有同分异构体,苯不能被酸性高锰酸钾氧化,苯不与溴水加成 | |
| D. | H2O 和H2O2 互为同素异形体. |
13.实验室进行下列反应时,需用水浴加热的是( )
①石油的分馏
②合成乙酸乙酯
③制取乙烯
④制硝基苯
⑤蔗糖水解
⑥葡萄糖溶液的银镜反应
⑦测定KNO3在80℃时的溶解度
⑧制溴苯⑨乙酸乙酯的水解.
①石油的分馏
②合成乙酸乙酯
③制取乙烯
④制硝基苯
⑤蔗糖水解
⑥葡萄糖溶液的银镜反应
⑦测定KNO3在80℃时的溶解度
⑧制溴苯⑨乙酸乙酯的水解.
| A. | ④⑤⑥⑦⑨ | B. | ③⑤⑥⑦⑧ | C. | ①②③⑤⑦ | D. | ②③⑤⑥⑦ |
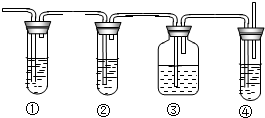 实验室里用乙醇和浓硫酸来制取乙烯:
实验室里用乙醇和浓硫酸来制取乙烯: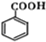 .
. (任选一种).
(任选一种).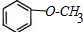 .
.