题目内容
在用C3H6(丙烯)合成C5H8O2(2-甲基丙烯酸甲酯)的过程中,欲使原子的利用率达到100%,在催化剂作用下,还需要的其他反应物是( )A.CH3OH和HBr B.CH3OH和H
D
解析:由丙烯合成2-甲基丙烯酸甲酯,从原子的个数来看,1个C3H6要增加C2H2O2才能得到C5H8O2,要使原子的利用率达到100%,所需物质的C、H、O个数比应为1∶1∶1,在这四个选项中,只有D项可能满足这个条件。

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目
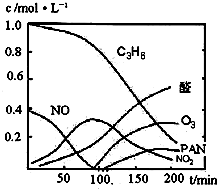 汽车尾气已经成为大气污染的主要污染源之一,某探究性学习小组的同学在一次社会实践中,到环保部门做了烟雾箱实验,他们起始时投入丙烯、NO及空气,用紫外线长时间照射气体,发生了一系列变化,用物质感应器数据采集器,通过计算机得出如图所示的变化曲线.结合曲线,试回答下列问题.
汽车尾气已经成为大气污染的主要污染源之一,某探究性学习小组的同学在一次社会实践中,到环保部门做了烟雾箱实验,他们起始时投入丙烯、NO及空气,用紫外线长时间照射气体,发生了一系列变化,用物质感应器数据采集器,通过计算机得出如图所示的变化曲线.结合曲线,试回答下列问题.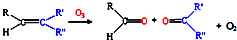 ,写出丙烯与臭氧作用生成醛的化学方程式(并配平)
,写出丙烯与臭氧作用生成醛的化学方程式(并配平)
 CH4(g)+HC≡CH(g)+H2(g);
△H1=156.6 kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g);
△H1=156.6 kJ·mol-1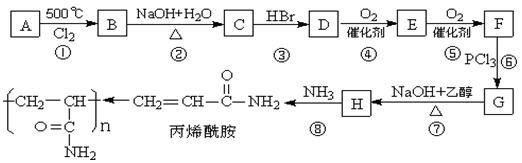
 ,写出丙烯与臭氧作用生成醛的化学方程式(并配平)______.
,写出丙烯与臭氧作用生成醛的化学方程式(并配平)______.