题目内容
11.bg某金属与足量的稀硫酸反应,生成该金属的三价正盐和a g氢气,则该金属的相对原子质量为$\frac{3b}{a}$.分析 某金属与足量的稀硫酸反应,生成该金属的三价正盐,设盐的化学式为R2(SO4)3,根据反应的化学方程式,由金属与生成氢气的质量关系,计算出金属的相对原子质量.
解答 解:设金属R的相对原子质量为m
2R+3H2SO4═R2(SO4)3+3H2↑
2m 3×2
bg ag
则m=$\frac{bg×3×2}{2×ag}$=$\frac{3b}{a}$;
故答案为:$\frac{3b}{a}$.
点评 本题考查了有关方程式的计算,题目难度不大,根据化合价写出硫酸盐的化学式和反应方程式是解题的关键,侧重于考查学生的分析能力和计算能力.

练习册系列答案
相关题目
1.下列离子方程式书写正确的是( )
| A. | 氯气溶于水:Cl2+H2O=2H++C1-+C1O- | |
| B. | 硫酸铝溶液中加入足量氨水:Al3++4OH-=AlO2-+2H2O | |
| C. | FeS04溶液与稀硝酸反应:3Fe2++NO3-+4H+=3Fe3++NO+2H2O | |
| D. | 稀硫酸中加入铁粉:2Fe+6H+═2Fe3++3H2↑ |
2.关于硫及其化合物说法正确的是( )
| A. | 自然界的硫元素主要以硫单质、硫化物和硫酸盐等形式存在 | |
| B. | 浓硫酸可作干燥剂,但不能干燥二氧化硫、氯气等气体 | |
| C. | 二氧化硫能使溴水褪色,说明其具有漂白性 | |
| D. | 浓硫酸中存在的主要是硫酸分子,常温下就能和铜片剧烈反应 |
6.下列涉及无机化合物的分离提纯,其中说法正确的是( )
| A. | 除去CO2中混有的少量SO2,可将气体通过酸性高锰酸钾溶液 | |
| B. | 除去SiO2中混有的少量Al2O3,可以用NaOH溶液洗涤 | |
| C. | 除去Fe粉中的少量Mg粉,可以将该粉末用稀硝酸洗涤,然后过滤 | |
| D. | 除去NO2气体中混有的少量NO气体,可以向该气体中充入过量空气 |
1.一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )
| A. | 反应进行60s时,X、Y、Z的浓度相等 | |
| B. | 反应进行80s时,逆反应速率大于正反应速率 | |
| C. | 以X浓度变化表示的反应速率为0.06mol/(L•min) | |
| D. | 反应进行80s时,Y物质的量浓度为0.03mol/L |
8.一种熔融碳酸盐燃料电池的工作原理如图.下列有关该电池的说法不正确的是( )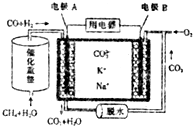

| A. | 电流方向:由B极经用电器流向A极 | |
| B. | 电极B上发生的电极反应为2CO2+O2+4e-═CO22- | |
| C. | 电池工作时,K+、Na+向电极B移动 | |
| D. | 若消耗电极B上的O233.6L(标准状况),则至少需要1moL CH4参加反应 |
5.已知NA为阿伏加德罗常数的值.有关草酸 (HOOC-COOH)的下列说法中错误的是( )
| A. | 9.0g草酸中共用电子对数目为0.9NA | |
| B. | 9.0 g草酸被NaClO氧化生成CO2,转移的电子数为0.2 NA | |
| C. | 9.0 g草酸溶于水,其中C2O42-和HC2O4-的微粒数之和为0.1NA | |
| D. | 9.0g草酸受热完全分解为CO2、CO、H2O,标况下测得生成的气体体积为4.48 L |