题目内容
【题目】钛(22Ti)由于其特殊的性能被誉为“未来世纪的金属”。钛铁矿主要成分为FeTiO3(含有少量MgO、SiO2等杂质),Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿来制备,工艺流程如下:

(1)Ti位于元素周期表中的位置为________。钛铁矿在预处理时需要进行粉碎,其原因是_______。
(2)过程①中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为80%时,所采用的实验条件是_________。

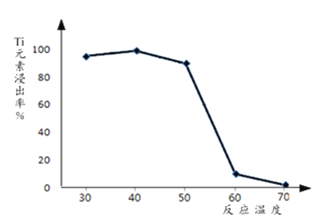
(3)过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示,反应温度过高时,Ti元素浸出率下降的原因是___________。
(4)写出由滤液D生成FePO4的离子方程式____________________________________。
(5)由流程图可知FePO4制备LiFePO4的化学方程式是_________________________。
【答案】第四周期IVB增大反应物接触面积,加快反应速率100℃ 3小时温度过高,双氧水分解与氨气逸出导致Ti元素浸出率下降2Fe2++ H2O2+ 2H3PO4 == 2FePO4 + 4H++ 2H2O2FePO4+ Li2CO3+ H2C2O4![]() 2LiFePO4+ 3CO2↑+ H2O
2LiFePO4+ 3CO2↑+ H2O
【解析】
(1)Ti的原子序数为22,处于第四周期第ⅣB族。钛铁矿在预处理时进行粉碎,增大了与盐酸的接触面积,可以加快反应速率。
(2)由图中三条曲线可得,当铁的浸出率为80%时,应为100℃、约浸取3小时。
(3)由于二氧化钛与氨水、双氧水反应生成(NH4)2Ti5O15时,温度过高,双氧水和氨水都容易分解(双氧水分解与氨气逸出),所以反应温度过高时,Ti元素浸出率下降。
(4)由流程可得,滤液D含有Fe2+,与H2O2、H3PO4反应,生成FePO4,离子方程式为:2Fe2++H2O2+2H3PO4=2FePO4+ 4H++2H2O。
(5)由流程图可知FePO4与H2C2O4、Li2CO3高温煅烧发生反应生成LiFePO4,铁的化合价降低,FePO4应为氧化剂,所以H2C2O4应为还原剂,故化学方程式为:2FePO4+Li2CO3+H2C2O4![]() 2LiFePO4+3CO2↑+H2O。
2LiFePO4+3CO2↑+H2O。

 名校课堂系列答案
名校课堂系列答案