题目内容
【题目】塑化剂主要用作塑料的增塑剂,也可作为农药载体、驱虫剂和化妆品等的原料。添加塑化剂(DBP)可改善白酒等饮料的口感,但超过规定的限量会对人体产生伤害。其合成线路图如图I所示:

已知以下信息:
①
②R1CHO + R2CH2CHO![]()
 +H2O(—R1、—R2表示氢原子或烃基)
+H2O(—R1、—R2表示氢原子或烃基)
③其中A的化学式是C8H10;C为含两个碳原子的烃的含氧衍生物,其核磁共振氢谱图如图II所示:峰的强度之比为2:1:3
请根据以上信息回答下列问题:
(1)C的结构简式为______, E中所含官能团的名称是_____________;
(2)写出下列有关反应的化学方程式:
①E和H2以物质的量比1︰1反应生成F:_______________________;
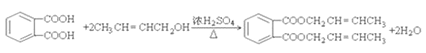
②B和F以物质的量比1︰2合成DBP:_______________________________,该反应的反应类型为__________________________。
【答案】 CH3CH2OH 醛基和碳碳双键 ![]()
 取代反应
取代反应
【解析】试题分析:A被高锰酸钾氧化为邻苯二甲酸,所以A是邻二甲苯;C为含两个碳原子的烃的含氧衍生物,其核磁共振氢谱图如图II所示:峰的强度之比为2:1:3,C是乙醇;D是乙醛;根据已知②,R1CHO + R2CH2CHO ![]() R1CH=CHCHO + H2O,可知E是CH3CH=CHCHO;E和H2以物质的量比1︰1反应生成F ,F是CH3CH=CHCH2OH;B与F发生酯化反应生成DBP;
R1CH=CHCHO + H2O,可知E是CH3CH=CHCHO;E和H2以物质的量比1︰1反应生成F ,F是CH3CH=CHCH2OH;B与F发生酯化反应生成DBP;
解析:根据以上分析,(1)C是乙醇,C的结构简式为CH3CH2OH, CH3CH=CHCHO中所含官能团的名称是醛基和碳碳双键;
(2)①E和H2以物质的量比1︰1反应生成的是CH3CH=CHCH2OH,方程式为![]() ;
;
②B和F以物质的量比1︰2发生酯化反应生成DBP的方程式为: ,该反应的反应类型为取代反应或酯化反应。
,该反应的反应类型为取代反应或酯化反应。

