题目内容
(10分)工业上对海水资源综合开发利用的部分工艺流程如下图所示。
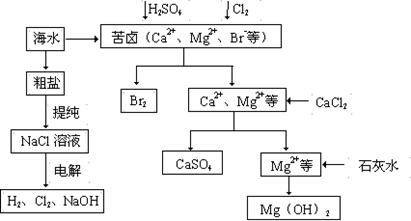
⑴ 粗盐中含有Ca2+、Mg2+、SO42-等杂质,粗制后可得饱和NaCl溶液,精制时通常在溶液中依次中加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出加入Na2CO3溶液后相关化学反应的离子方程式:
、 。
⑵ 从海水中提取溴,主要反应为2Br- + Cl2 = Br2 + 2Cl-,下列说法错误的是 (填序号)。
⑶ 本工艺流程中先后制得Br2、CaSO4、Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备?
(填“能”或“否”),原因是 。

⑴ 粗盐中含有Ca2+、Mg2+、SO42-等杂质,粗制后可得饱和NaCl溶液,精制时通常在溶液中依次中加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出加入Na2CO3溶液后相关化学反应的离子方程式:
、 。
⑵ 从海水中提取溴,主要反应为2Br- + Cl2 = Br2 + 2Cl-,下列说法错误的是 (填序号)。
| A.溴离子具有氧化性 | B.氯气是还原剂 |
| C.该反应属于复分解反应 | D.Br2是氧化产物 |
(填“能”或“否”),原因是 。
⑴ Ca2+ + CO32- = CaCO3↓、Ba2+ + CO32- = BaC O3↓ (各2分,共4分)
O3↓ (各2分,共4分)
⑵ ABC (3分)
⑶ 否(1分)如果先沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,产品不纯 (2分)
 O3↓ (各2分,共4分)
O3↓ (各2分,共4分)⑵ ABC (3分)
⑶ 否(1分)如果先沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,产品不纯 (2分)
略

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 用铁矿石炼铁、用氨制碳酸铵都会产生温室气体
用铁矿石炼铁、用氨制碳酸铵都会产生温室气体 68变为4.28,是因为水中溶解了较多的CO2
68变为4.28,是因为水中溶解了较多的CO2 ,将乙针筒内的物质压到甲针筒内,进行下表所列的不伺实验(气体在同温同压下测定)。
,将乙针筒内的物质压到甲针筒内,进行下表所列的不伺实验(气体在同温同压下测定)。

 的化学方程式 。
的化学方程式 。 在空气中浓度降低
在空气中浓度降低 久置后均会变质
久置后均会变质