��Ŀ����
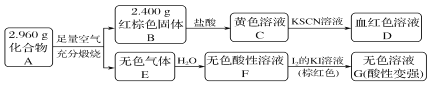
����Ŀ�����Բ���A��������Ԫ����ɵĻ����ij�о�С�鰴��ͼ����̽������ɣ�
��ش�
��1��A�����Ԫ��Ϊ________(��Ԫ�ط��ű�ʾ)����ѧʽΪ_____________________��
��2����ҺC���ܽ�ͭƬ�����ٸ÷�Ӧ��һ��ʵ��Ӧ��________��
��3����֪������A����ϡ���ᷴӦ������һ�ֵ���ɫ�������һ������(����µ��ܶ�Ϊ1.518 g��L��1)����������ӵĵ���ʽΪ________��д���÷�Ӧ�����ӷ���ʽ____________________��
д��F��G��Ӧ�Ļ�ѧ����ʽ___________________________________��
���ʵ�鷽��̽����ҺG�е���Ҫ��(������H2O��H����K����I��) _____________________��
���𰸡� S��Fe Fe3S4 ��ӡˢ��·�� ![]() Fe3S4��6H��===3Fe2����3H2S����S H2SO3��I2��H2O=H2SO4��2HI ȡ��ҺG���������BaCl2��Һ����������ɫ����������SO42�������˺�ȡ��Һ���μ�H2O2��Һ�����ٲ�����ɫ����������H2SO3
Fe3S4��6H��===3Fe2����3H2S����S H2SO3��I2��H2O=H2SO4��2HI ȡ��ҺG���������BaCl2��Һ����������ɫ����������SO42�������˺�ȡ��Һ���μ�H2O2��Һ�����ٲ�����ɫ����������H2SO3
��������C����KSCN��DΪѪ��ɫ��Һ����֪CΪFeCl3��DΪFe(SCN)3 �ȣ���֪BΪFe2O3����n��Fe2O3��=2.400g/160g��mol��1=0.015mol��n��Fe��=0.03mol��m��Fe��=0.03mol��56g��mol��1=1.68g��Aȼ�����ɵ���ɫ����E��Һˮ�õ�������Һ��������KI��Һ���õ���ɫ��Һ��˵���������E��ˮ��Һ��EӦΪSO2��FΪH2SO3��G���к�H2SO4��HI����֪A����Fe��SԪ�أ���m��S��=2.96g-1.68g=1.28g��n��S��=1.28g/32g��mol��1=0.04mol����֪n��Fe����n��S��=3��4��ӦΪFe3S4����1�������Ϸ�����֪��A���Ԫ��ΪFe��S��ΪFe3S4����2�������Ӿ���ǿ�����ԣ��ɽ�ͭ��������������ӡˢ��·�壻��3��������A����ϡ���ᷴӦ������һ�ֵ���ɫ�������һ�����壨����µ��ܶ�Ϊ1.518 g��L��1��������ɫ������ΪS���������Է�������Ϊ1.518��22.4L=34��ΪH2S���壬����ʽΪ![]() ����Ӧ�����ӷ���ʽΪFe3S4+6H��=3Fe2��+S+3H2S������4��F��G��Ӧ�Ļ�ѧ����ʽΪH2SO3+I2+H2O=H2SO4+2HI����ҺG�е���Ҫ����������H2O��H����K����I���� ΪSO42����H2SO3�����ȼ���SO42�����������H2SO3���������Ϊ��ȡ��ҺG���������BaCl2��Һ����������ɫ����������SO42�������˺�ȡ��Һ���μ�H2O2��Һ�����ٲ�����ɫ����������H2SO3��
����Ӧ�����ӷ���ʽΪFe3S4+6H��=3Fe2��+S+3H2S������4��F��G��Ӧ�Ļ�ѧ����ʽΪH2SO3+I2+H2O=H2SO4+2HI����ҺG�е���Ҫ����������H2O��H����K����I���� ΪSO42����H2SO3�����ȼ���SO42�����������H2SO3���������Ϊ��ȡ��ҺG���������BaCl2��Һ����������ɫ����������SO42�������˺�ȡ��Һ���μ�H2O2��Һ�����ٲ�����ɫ����������H2SO3��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����֪��ӦA(g)+B(g)![]() C(g)+D(g)��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/�� | 700 | 800 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
��ش��������⣺
(1)�÷�Ӧƽ�ⳣ������ʽΪK=_______����H=_______0��ѡ�>������<����=������
(2)830��ʱ����һ��5L���ܱ������г���0.40mol��A��0.60mol��B����Ӧ��6minʱ�ﵽƽ��״̬��
�ٸö�ʱ����A��ƽ����Ӧ����v(A)=__________���ﵽƽ��ʱB��ת����Ϊ_________��
��������ʱ������ϵ�����ͷ�48kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ��_________��
�۴�ʱ����ܱ������г���1mol�����ƽ��ʱA��ת����_______��ѡ���������С���������䡱����
(3)�жϸ÷�Ӧ�ﵽƽ�������Ϊ_________������ȷѡ�����ĸ����
a��ѹǿ����ʱ��ı� b��������ܶȲ���ʱ��ı�
c��c(A)����ʱ��ı� d����λʱ��������C��D�����ʵ������
e����λʱ��������amolA��ͬʱ������amolB
(4)1200��ʱ��ӦC(g)+D(g)![]() A(g)+B(g)��ƽ�ⳣ����ֵΪ_________��
A(g)+B(g)��ƽ�ⳣ����ֵΪ_________��