题目内容
(8分)非金属单质及其化合物在生产和科研中都有重要应用。
(1) 若发生大量氯气泄漏事故,下列措施中正确的是_________。
a.立即通报相关部门,迅速撤离事故现场
b.用蘸有肥皂水的毛巾捂住口鼻立即逆风疏散
c.用蘸有NaOH溶液的毛巾捂住口鼻立即顺风疏散
(2) 事故发生后,可用NaOH稀溶液处理泄漏的氯气,反应的离子方程式是________。
(3) 向Na2SO3和Na2S的混合溶液中加入稀盐酸,溶液中会产生大量淡黄色沉淀。则该反应中氧化剂和还原剂的物质的量之比是__________
(4) Cl2与NO2在一定条件下发生化合反应,生成一种气体,实验数据如图。图中横坐标是加入C12的物质的量,纵坐标是反应后气体物质的量总和。已知所取C12、NO2的物质的量总和为6 mol。则生成物的化学式是__________。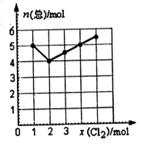
(1) 若发生大量氯气泄漏事故,下列措施中正确的是_________。
a.立即通报相关部门,迅速撤离事故现场
b.用蘸有肥皂水的毛巾捂住口鼻立即逆风疏散
c.用蘸有NaOH溶液的毛巾捂住口鼻立即顺风疏散
(2) 事故发生后,可用NaOH稀溶液处理泄漏的氯气,反应的离子方程式是________。
(3) 向Na2SO3和Na2S的混合溶液中加入稀盐酸,溶液中会产生大量淡黄色沉淀。则该反应中氧化剂和还原剂的物质的量之比是__________
(4) Cl2与NO2在一定条件下发生化合反应,生成一种气体,实验数据如图。图中横坐标是加入C12的物质的量,纵坐标是反应后气体物质的量总和。已知所取C12、NO2的物质的量总和为6 mol。则生成物的化学式是__________。

(1)a、b(2分)(2)Cl2+2OH-=Cl-+ClO-+H2O(2分)(3)1:2(2分)(4)NO2Cl(2分)
略

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
 3
3 )写出电解CE溶液的化学方程式:
)写出电解CE溶液的化学方程式: 本题共7分)
本题共7分)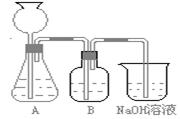
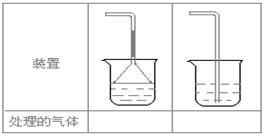
 (5)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理,并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。
(5)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理,并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。