题目内容
【题目】下列说法正确的是:
A.在100℃、101KPa条件下,液态水的气化热为40.69kJ/mol,则H2O(g)![]() H2O(l)的 △H= 40.69kJ/mol
H2O(l)的 △H= 40.69kJ/mol
B.已知MgCO3的Ksp =6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)·c(CO32-)=6.82×10-6
C.己知:
则可以计算出反应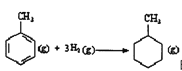 的△H为-384kJ·mol-1
的△H为-384kJ·mol-1
D.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的pH 减小
【答案】D
【解析】
试题分析:A.液态水的气化热为40.69kJ/mol-1,是液体水变化为气体需要吸收热量,焓变为负值,故A错误;B.含有固体MgCO3的溶液中,Mg2+和CO32-离子浓度可能不相等,如在MgCl2和Na2CO3溶液中,并且在不同的温度下,溶度积常数不同,故B错误;C.因为苯环中的碳碳键是介于单双键之间的一种独特的键,不存在典型的碳碳双键和碳碳单键,不能用以上表中进行计算,故C错误;D.NH3·H2O溶液中加入少量NH4Cl晶体,NH4+浓度增大使电离平衡向逆方向移动,电离程度降低,溶液pH的减小,故D正确。

练习册系列答案
相关题目
【题目】100mL 1mol![]() 的Ca(HCO3)2溶液中,放入2.3g金属钠充分反应后,有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
的Ca(HCO3)2溶液中,放入2.3g金属钠充分反应后,有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
生成CaCO3 | 溶液中 | H2 | 转移的电子 | |
A | 0.1NA | 0.1NA | ||
B | 1.12L | 0.1NA | ||
C | 10g | 0.05NA | ||
D | 10g | 0.1NA |

