题目内容
下列对离子方程式评价正确的是( )
|
分析:A.反应生成亚铁离子和氢气;
B.硝酸具有氧化性,反应生成铁离子和水;
C.电子不守恒;
D.FeBr2溶液与Cl2以2:3反应,亚铁离子、溴离子全部被氧化.
B.硝酸具有氧化性,反应生成铁离子和水;
C.电子不守恒;
D.FeBr2溶液与Cl2以2:3反应,亚铁离子、溴离子全部被氧化.
解答:解:A.将铁粉加入硫酸氢钠溶液中的离子反应为Fe+2H+═Fe2++H2↑,评价错误,故A错误;
B.将磁性氧化铁溶于足量稀硝酸中的离子反应为3Fe3O4+NO3-+28H+═9Fe3++14H2O+NO↑,评价错误,故B错误;
C.向硝酸亚铁溶液中滴加盐酸的离子反应为3Fe2++4H++NO3-═3Fe3++NO↑+2H2O,评价正确,故C正确;
D.FeBr2溶液与Cl2以2:3反应的离子反应为2Fe2++4Br-+3Cl2═2Fe3+,+2Br2+6Cl-,评价错误,故D错误;
故选C.
B.将磁性氧化铁溶于足量稀硝酸中的离子反应为3Fe3O4+NO3-+28H+═9Fe3++14H2O+NO↑,评价错误,故B错误;
C.向硝酸亚铁溶液中滴加盐酸的离子反应为3Fe2++4H++NO3-═3Fe3++NO↑+2H2O,评价正确,故C正确;
D.FeBr2溶液与Cl2以2:3反应的离子反应为2Fe2++4Br-+3Cl2═2Fe3+,+2Br2+6Cl-,评价错误,故D错误;
故选C.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意氧化还原反应中电子守恒,选项D为易错点,题目难度中等.

练习册系列答案
相关题目
下列是某同学对相应反应的离子方程式所作的评价,其中评价完全合理的是( )
|
下列对离子方程式书写评价正确的是
| 选项 | 化学反应与离子方程式 | 评价 |
| A | 将铜屑加入Fe3+溶液中:Fe3++Cu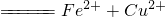 | 正确 |
| B | Na2O2与H2O反应Na2O2+H2O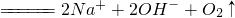 | 错误,氧元素不守恒 |
| C | NaOH溶液与氧化铝反应:Al2O3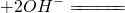 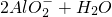 | 错误,产物应该是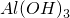 |
| D | 向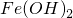 中加入足量稀硝酸: 中加入足量稀硝酸: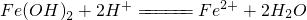 | 正确 |
- A.A
- B.B
- C.C
- D.D
下列对离子方程式评价正确的是
| 选项 | 化学反应 | 离子方程式 | 评价 |
| A | 将铁粉加入硫酸氢钠溶液中 | 2Fe+6H+═2Fe3++3H2↑ | 正确 |
| B | 将磁性氧化铁溶于足量稀硝酸中 |  ═2Fe3++Fe2++4H2O ═2Fe3++Fe2++4H2O | 正确 |
| C | 向硝酸亚铁溶液中滴加盐酸 | Fe2++4H++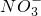 ═Fe3++NO↑+2H2O ═Fe3++NO↑+2H2O | 错误,得失电子和电荷都不守恒 |
| D | FeBr2溶液与Cl2以2:3反应 | 2 ═2Fe3++Br2+4Cl- ═2Fe3++Br2+4Cl- | 正确 |
- A.A
- B.B
- C.C
- D.D