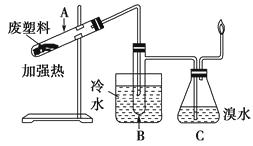
��Ŀ����
����Ŀ����֪��2NO2��g��N2O4��g����H��0���ں��º��������£���һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������У���Ӧ�����и����ʵ���Ũ��c��ʱ��t�ı仯��ϵ��ͼ��ʾ�� 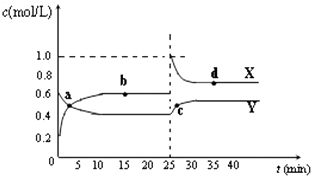
��1��a��b��c��d�ĸ����У���ѧ��Ӧ����ƽ��״̬�����㣮
��2��25minʱ���������������ʵĻ�ѧʽ��mol��
��3��a��b��c��d�ĸ���������ʾ�ķ�Ӧ��ϵ�У�������ɫ���dz��˳����������ĸ����
���𰸡�
��1��b��d
��2��NO2��0.8
��3��cdba
���������⣺��ͼ��֪10��25minƽ��״̬ʱ��X��ʾ���������Ũ�ȱ仯��Ϊ��0.6��0.2��mol/L=0.4mol/L��Y��ʾ�ķ�Ӧ���Ũ�ȱ仯��Ϊ��0.6��0.4��mol/L=0.2mol/L��X��ʾ���������Ũ�ȱ仯����Y��ʾ�ķ�Ӧ���Ũ�ȱ仯����2��������X��ʾNO2Ũ����ʱ��ı仯���ߣ�Y��ʾN2O4Ũ����ʱ��ı仯���ߣ���1����ͼ֪��10��25min��35min֮��X��Y�����ʵ����������仯������Ӧʱ����ڵĵ㴦�ڻ�ѧƽ��״̬����b��d���ڻ�ѧƽ��״̬�����Դ��ǣ�b��d����2��25minʱ��c��NO2��˲������ƽ��״̬�����ˣ�1��0.6����2=0.8mol ����c��NO2����ƽ��������N2O4�����ƶ������Դ��ǣ�NO2��0.8����3����a��b��c��NO2������c���d��ֱ�������c��NO2����δ�ﵽƽ��ĵ��ƽ��ʱ�ĵ㣬����c��c��NO2������d�㣬��������Ũ��Խ����ɫԽ�����ɫ���dz��˳����cdba�����Դ��ǣ�cdba��
�����㾫����������Ŀ����֪���������û�ѧƽ��״̬���ʼ����������֪ʶ���Եõ�����Ĵ𰸣���Ҫ���ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч����