题目内容
已知A、B、C三种元素均为短周期元素,它们的原子序数关系为:C>B>A,A元素原子的最外层电子数是次外层电子数的2倍,B和C可形成BC4型化合物。用化学符号填空:(1)三种元素中A是_______、B是_______、C是_______。
(2)A、B、C的最高价氧化物对应的水化物分别是_______、_______、_______,在这些水化物中,酸性最弱的是_______。
(3)BC4的电子式是_______。
(4)已知BC4不能在空气中燃烧,理由是_______。
(6)用离子方程式表示出用B的氧化物制得B的氧化物对应水化物的原理。
答案:
解析:
解析:
| (1)C Si Cl
(2)H2CO3 H2SiO3 HClO4 H2SiO3 (3) (4)SiCl4在点燃的条件下不能被O2氧化 (5)SiO2+2OH-====SiO32-十H2O
SiO
|

练习册系列答案
相关题目

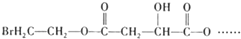
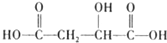

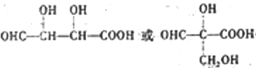
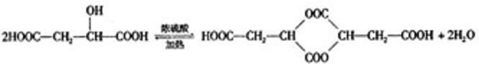
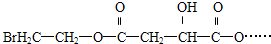
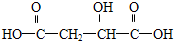 试回答:
试回答:
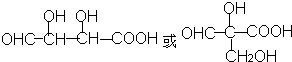
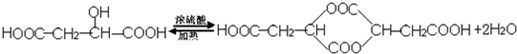
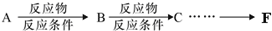
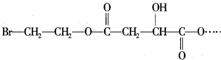
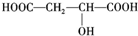

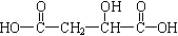 ,
,