题目内容
【题目】下图是中学化学中常用于化合物的分离和提纯装置,请根据装置回答问题:
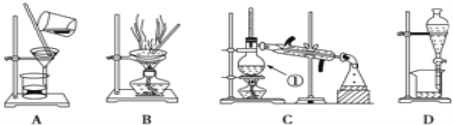
下图是中学化学中常用于化合物的分离和提纯装置,请根据装置回答问题:
(1)装置B中被加热仪器的名称是_____,装置C中①的名称是_________。
(2)某硝酸钠固体中混有少量硫酸钠杂质,现设计一实验方案,既除去杂质,又配成硝酸钠溶液。
实验方案:先将固体溶于蒸馏水配成溶液,选择合适的试剂和操作完成表格中各步实验。
选择试剂 | ① | Na2CO3溶液 | ④ |
实验操作 | ② | ③ | 加热 |
所加入的试剂①可以是_____(填化学式),证明溶液中SO42-已经除尽的操作是__________。加入Na2CO3溶液的目的是__________,所加入的试剂④是____________ (填化学式)。
(3)青蒿素是高效的抗疟疾药,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为:
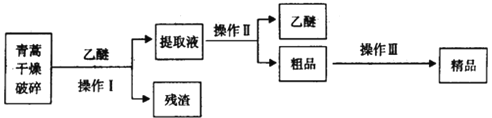
若要在实验室模拟上述工艺,操作I选择的实验操作是_____,操作Ⅱ选择的实验操作是_________。
【答案】蒸发皿 蒸馏烧瓶 Ba(NO3)2或Ba(OH)2 静置,向上层清液中继续滴加Ba(NO3)2或者是Ba(OH)2,若无沉淀产生则已除尽 除去过量的Ba2+ HNO3 过滤 蒸馏
【解析】
(1)装置B中被加热仪器的名称是蒸发皿,装置C中①的名称是蒸馏烧瓶。
(2)某硝酸钠固体中混有少量硫酸钠杂质,可加入Ba(NO3)2或者Ba(OH)2除去SO42-,同时需考虑过量Ba2+的处理,显然应加入Na2CO3,过量的Na2CO3应使用HNO3进行处理。
检验溶液中SO42-是否已经除尽时,可向上层清液中继续滴加Ba(NO3)2或Ba(OH)2,看是否有沉淀生成。
(3)从图中可以看出,操作I是固液分离的操作,操作Ⅱ是分离两种互溶有机物的操作。
(1)装置B中被加热仪器的名称是蒸发皿,装置C中①的名称是蒸馏烧瓶。答案为:蒸发皿;蒸馏烧瓶;
(2)某硝酸钠固体中混有少量硫酸钠杂质,可加入Ba2+除去SO42-,同时需考虑过量Ba2+的处理,显然应加入CO32-,过量的CO32-应使用HNO3进行处理。
综合以上分析可知,所加入的试剂①可以是Ba(NO3)2或者是Ba(OH)2,证明溶液中SO42-已经除尽的方法是静置,向上层清液中继续滴加Ba(NO3)2或者是Ba(OH)2,若无沉淀产生则已除尽。加入Na2CO3溶液的目的是除去过量的Ba2+;,所加入的试剂④可以是HNO3。
答案为:Ba(NO3)2或者是Ba(OH)2;静置,向上层清液中继续滴加Ba(NO3)2或者是Ba(OH)2,若无沉淀产生则已除尽;除去过量的Ba2+;HNO3。
(3)从图中可以看出,操作I是固液分离的操作,即为过滤,操作Ⅱ是分离两种互溶有机物的操作,即为蒸馏。答案为:过滤;蒸馏。

 优加精卷系列答案
优加精卷系列答案