题目内容
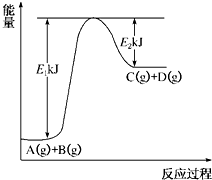 已知某反应A(g)+B(g)?C(g)+D(g)进行过程中的能量变化如图所示,请回答下列问题:
已知某反应A(g)+B(g)?C(g)+D(g)进行过程中的能量变化如图所示,请回答下列问题:(1)该反应的△H=
(2)若在反应体系中加入催化剂使逆反应速率增大,则E1
(3)在相同温度和压强下,对反应A(g)+B(g)?C(g)+D(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
| A | B | C | D | |
| 甲 | a mol | a mol | 0 | 0 |
| 乙 | 2a mol | a mol | 0 | 0 |
| 丙 | a mol | a mol | a mol | a mol |
| 丁 | a mol | 0 | a mol | a mol |
A.甲=丙>乙=丁 B.乙>丁>甲>丙 C.丁>乙>甲=丙 D.丙>乙=丁>甲
(4)若上述反应达到平衡,为了提高A的转化率,可以采用的措施有(写一条):
(5)在恒温恒容条件下进行上述反应.下列情况可以判断该反应达到平衡状态的是
A.气体平均摩尔质量不再变化 B.气体压强不再变化
C.气体密度不再变化 D.消耗A的速率等于消耗D的速率
E.各组分浓度之比为1:1:1:1 F.C生成的速率等于B消耗的速率.
分析:(1)反应的焓变△H=E1-E2;
(2)加催化剂降低反应的活化能,催化剂不能改变反应物的总能量与生成物总能量之差,即反应热不变;
(3)在相同温度和压强下的可逆反应,反应后气体体积不变,按方程式的化学计量关系转化为方程式同一边的物质进行分析;
(4)提高A的转化率,即平衡正移;
(5)可根据化学平衡状态的概念和化学平衡状态的特征“等”和“定”来分析解答.
(2)加催化剂降低反应的活化能,催化剂不能改变反应物的总能量与生成物总能量之差,即反应热不变;
(3)在相同温度和压强下的可逆反应,反应后气体体积不变,按方程式的化学计量关系转化为方程式同一边的物质进行分析;
(4)提高A的转化率,即平衡正移;
(5)可根据化学平衡状态的概念和化学平衡状态的特征“等”和“定”来分析解答.
解答:解:(1)反应的焓变△H=E1-E2,故答案为:E1-E2;
(2)加催化剂降低反应的活化能,催化剂不能改变反应物的总能量与生成物总能量之差,即反应热不变,故答案为:减小;不变;
(3)假设丙、丁中的CO、H2O(g)全部转化为CO2、H2,再与甲、乙比较:
A(g)+B(g) C(g)+D(g)
C(g)+D(g)
丙开始时 amol amol amol amol
丙假设全转化 2amol 2amol 0mol 0mol
丁开始时 amol 0mol amol amol
丁假设全转化 2amol amol 0mol 0mol
通过比较,甲中A为amol、B为amol;乙中A为2amol、B为amol;丙中A为2amol、B为2amol;丁中A为2amol、B为amol;乙、丁的数值一样,且乙、丁的数值大于甲,丙的数值大于乙、丁,反应物的量越多,生成的D越多,所以C(D)的大小顺序是:丙>乙=丁>甲;
故答案为:D;
(4)要提高A的转化率,即平衡正移,可知增大B 的浓度;故答案为:增大B的浓度;
(5)A.反应前后气体的物质的量不变,气体的质量不变,所以气体平均摩尔质量始终不变化,所以不能判断平衡状态,故错误;
B.反应前后气体的物质的量不变,所以气体压强始终不变化,所以不能判断平衡状态,故错误;
C.反应前后气体的体积不变,气体的质量不变,所以气体密度始终不变化,所以不能判断平衡状态;
D.消耗A的速率为正速率,消耗D的速率为逆速率,而且A和D的计量数相等,所以消耗A的速率等于消耗D的速率,即正速率等于逆速率属于平衡状态,故正确;
E.各组分浓度之比为1:1:1:1 不能判断平衡状态,故错误;
F.C生成的速率为正速率,B消耗的速率为正速率,都是正速率,所以不能判断平衡状态,故错误;
故答案为:D.
(2)加催化剂降低反应的活化能,催化剂不能改变反应物的总能量与生成物总能量之差,即反应热不变,故答案为:减小;不变;
(3)假设丙、丁中的CO、H2O(g)全部转化为CO2、H2,再与甲、乙比较:
A(g)+B(g)
 C(g)+D(g)
C(g)+D(g)丙开始时 amol amol amol amol
丙假设全转化 2amol 2amol 0mol 0mol
丁开始时 amol 0mol amol amol
丁假设全转化 2amol amol 0mol 0mol
通过比较,甲中A为amol、B为amol;乙中A为2amol、B为amol;丙中A为2amol、B为2amol;丁中A为2amol、B为amol;乙、丁的数值一样,且乙、丁的数值大于甲,丙的数值大于乙、丁,反应物的量越多,生成的D越多,所以C(D)的大小顺序是:丙>乙=丁>甲;
故答案为:D;
(4)要提高A的转化率,即平衡正移,可知增大B 的浓度;故答案为:增大B的浓度;
(5)A.反应前后气体的物质的量不变,气体的质量不变,所以气体平均摩尔质量始终不变化,所以不能判断平衡状态,故错误;
B.反应前后气体的物质的量不变,所以气体压强始终不变化,所以不能判断平衡状态,故错误;
C.反应前后气体的体积不变,气体的质量不变,所以气体密度始终不变化,所以不能判断平衡状态;
D.消耗A的速率为正速率,消耗D的速率为逆速率,而且A和D的计量数相等,所以消耗A的速率等于消耗D的速率,即正速率等于逆速率属于平衡状态,故正确;
E.各组分浓度之比为1:1:1:1 不能判断平衡状态,故错误;
F.C生成的速率为正速率,B消耗的速率为正速率,都是正速率,所以不能判断平衡状态,故错误;
故答案为:D.
点评:本题考查反应热的判断,影响化学反应速率和平衡的因素,难度适中,根据所学知识即可完成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(8分) 已知某反应A(g)+B(g)⇌C(g)+D(g)进行过程中的能量变化如图所示,请回答下列问题:

(1)该反应的ΔH=________kJ·mol-1(用含E1、E2的代数式表示)。(1分)
(2)若在反应体系中加入催化剂使逆反应速率增大,则E1________(填“增大”、“减小”或“不变”,下同),ΔH________。(2分)
(3)在相同温度和压强下,对反应A(g)+B(g)??C(g)+D(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
|
|
A |
B |
C |
D |
|
甲 |
a mol |
a mol |
0 |
0 |
|
乙 |
2a mol |
a mol |
0 |
0 |
|
丙 |
a mol |
a mol |
a mol |
a mol |
|
丁 |
a mol |
0 |
a mol |
a mol |
上述四种情况达到平衡后,C(D)的大小顺序是________。(2分)
A.乙=丁>丙=甲 B.乙>丁>甲>丙 C.丁>乙>丙=甲 D.丁>丙>乙>甲
(4)若上述反应达到平衡,为了提高A的转化率,可以采用的措施有(写一条):________________________________________________________________________。(1分)
(5)在恒温恒容条件下进行上述反应。下列情况可以判断该反应达到平衡状态的是____(2分)
A.气体平均摩尔质量不再变化 B. 气体压强不再变化
C. 气体密度不再变化 D. 消耗A的速率等于消耗D的速率
E. 各组分浓度之比为1:1:1:1 F. C生成的速率等于B消耗的速率
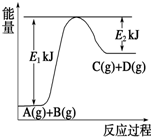 Ⅰ.已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.
Ⅰ.已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题. 已知某反应A(g)+B(g)?C(g)+D(g) 过程中的能量变化如图所示,回答下列问题.
已知某反应A(g)+B(g)?C(g)+D(g) 过程中的能量变化如图所示,回答下列问题.