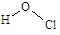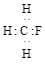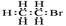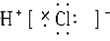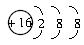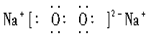题目内容
下列各项中表达不正确的是
A.F-的结构示意图: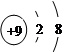 |
B.NaCl的电子式: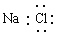 |
| C.CO2的分子结构式: O=C=O |
| D.碳-12原子 |
B
试题分析:氯化钠是离子化合物,含有离子键,电子式是
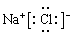 ,选项B不正确,其余选项都是正确的,答案选B。
,选项B不正确,其余选项都是正确的,答案选B。点评:该题是中等难度的试题,也是高考中的常见题型与重要的考点。该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度。该类试题需要明确的是常见的化学用语主要包括元素符号、化学式、化合价、电子式、原子结构示意图、结构式、结构简式以及方程式和各种模型等,需要学生熟练记住,并能灵活运用。

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目

 2K2Cr2O7+4KOH+2H2↑+O2↑已知K2CrO4铬酸钾溶液中存在平衡:2CrO42-(黄色)+2H+
2K2Cr2O7+4KOH+2H2↑+O2↑已知K2CrO4铬酸钾溶液中存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O通电后阳极区溶液由 变为 。原因是 。
Cr2O72-(橙色)+H2O通电后阳极区溶液由 变为 。原因是 。
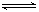 Ba2+(aq)+SO42-(aq)
Ba2+(aq)+SO42-(aq) 2CrO42-+2H+
2CrO42-+2H+ 2Al+Fe2O3
2Al+Fe2O3