题目内容
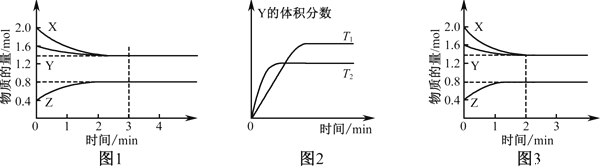
【题目】T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2(T2>T1)时,Y的体积分数(或Y的物质的量分数)与时间的关系如图2所示。则下列结论正确的是( )
A. 容器中发生的反应可表示为:4X(g)+Y(g)![]() 2Z(g)
2Z(g)
B. 反应进行的前3min内,用X表示的反应速率v(X)=0.3mol/(L·min)
C. 升高温度,反应的化学平衡常数K增大
D. 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
【答案】C
【解析】A. 根据图1可知,反应达到平衡时,X、Y分别减小了0.6mol和0.2mol,Z增加了0.4mol,由于在反应中反应物减小,生成物增加,且反应物减少的物质的量和生成物增加的物质的量之比等于化学计量数之比,所以该反应的化学方程式为3X(g)+Y(g)![]() 2Z(g),故A错误;B. 根据v=
2Z(g),故A错误;B. 根据v=![]() 可计算出反应速率v(X)=
可计算出反应速率v(X)=![]() =0.1mol/(L·min),故B错误;C. 根据图2可知,“先拐先平数值大”,所以T2>T1,当升高温度时,Y的体积分数减小,则平衡正向移动,所以平衡常数增大,故C正确;D. 比较图1和图3可知,图3时平衡没有移动,但反应速率加快,由于该反应是前后体积减小的反应,增大压强,平衡将会正向移动,故应为使用催化剂,故D错误;答案选C。
=0.1mol/(L·min),故B错误;C. 根据图2可知,“先拐先平数值大”,所以T2>T1,当升高温度时,Y的体积分数减小,则平衡正向移动,所以平衡常数增大,故C正确;D. 比较图1和图3可知,图3时平衡没有移动,但反应速率加快,由于该反应是前后体积减小的反应,增大压强,平衡将会正向移动,故应为使用催化剂,故D错误;答案选C。

练习册系列答案
相关题目