题目内容
【题目】乙酸乙酯是一种非常重要的有机化工原料,用途十分广泛.根据所学内容填空。
I.由乙烯合成乙酸乙酯的流程如下;
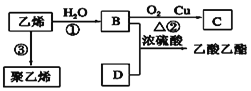
(1)写出B与D反应的化学方程式________;反应类型:_________;
(2)写出反应③的化学方程式:_________。
II.实验室用如图所示装置制备乙酸乙酯.
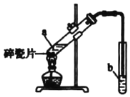
(1)实验前,向试管a中加入3mL______,然后边振荡试管边慢慢加入2mL______和2mL乙酸。
(2)试管b中盛放的试剂是饱和_____溶液。试管b中的导管不能伸入液面下的原因是____。
(3)反应结東后,从试管b中分离出乙酸乙酯的方法是______。
(4)下列描述不能说明乙醇与乙酸的反应已达到化学平衡状态的有_____(填序号)。
a.单位时间里,生成lmol乙酸乙酯,同时生成lmol水
b.单位时间区,生成lmol乙酸乙酯,同时生成1mol乙酸
c.单位时间里,消耗lmol乙醇,同时消耗1mol乙酸
d.正反应的速率与逆反应的速率相等
e.混合物中各物质的浓度不再变化
【答案】CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 酯化反应或取代反应 nCH2=CH2
CH3COOCH2CH3+H2O 酯化反应或取代反应 nCH2=CH2![]()
![]() 乙醇 浓硫酸 碳酸钠 防止倒吸 分液 ac
乙醇 浓硫酸 碳酸钠 防止倒吸 分液 ac
【解析】
乙烯和水发生加成反应制得B为乙醇,乙醇在铜做催化剂的条件下反应制得C乙醛,乙醇和D乙酸在浓硫酸作催化剂的条件下反应制得乙酸乙酯,乙烯发生加聚反应制得聚乙烯;实验室制取乙酸乙酯的实验操作为:实验前,向试管a中加入3mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL乙酸,用饱和碳酸钠溶液吸收乙酸乙酯,据此分析。
(1) B乙醇与D乙酸在浓硫酸作催化剂的条件下反应生成乙酸乙酯,化学方程式CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;反应类型:酯化反应或取代反应;
CH3COOCH2CH3+H2O;反应类型:酯化反应或取代反应;
(2)反应③是乙烯发生加聚反应制得聚乙烯,化学方程式为:nCH2=CH2![]()
![]() ;
;
II. (1)实验室用如图所示装置制备乙酸乙酯时,由于浓硫酸的密度较大,溶于水放出大量的热,实验前,向试管a中加入3mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL乙酸;
(2)制取的乙酸乙酯和挥发出的乙酸和乙醇一起蒸出,试管b中盛放的试剂是饱和碳酸钠溶液,可以溶解乙醇,吸收乙酸,降低乙酸乙酯的溶解度,试管b中的导管不能伸入液面下的原因是防止倒吸;
(3)反应结東后,制得的乙酸乙酯和饱和碳酸钠溶液是互不相溶的,是分层的,从试管b中分离出乙酸乙酯的方法是分液;
(4) a.单位时间里,生成lmol乙酸乙酯,同时生成lmol水,都代表正反应方向的速率,不能代表达到化学平衡,故a符合题意;
b.单位时间区,生成lmol乙酸乙酯,同时生成1mol乙酸,代表的是正逆反应速率相等,证明达到化学平衡,故b不符合题意;
c.单位时间里,消耗lmol乙醇,同时消耗1mol乙酸,都代表正反应方向速率,不能代表达到化学平衡,故c符合题意;
d.正反应的速率与逆反应的速率相等代表达到化学平衡,故d不符合题意;
e.混合物的各物质的浓度是一个变值,混合物中各物质的浓度不再变化,代表达到化学平衡,故e不符合题意;
答案选ac。

 名校课堂系列答案
名校课堂系列答案【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:
(1)选用的指示剂是______________________。
(2)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视______________________。
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,请将数据填入下面表格的横线处。
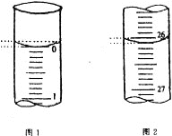
滴定次数 | 待测氢氧化钠溶液的体积/ mL | 0.1000 mol/L 盐酸的体积/ mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/ mL | ||
第一次 | 25.00 | 0.00 | ________ | _______ |
第二次 | 25.00 | 2.00 | 28.08 | 26.08 |
第三次 | 25.00 | 0.22 | 26.34 | 26.12 |
(5)请根据上表中数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)= _________。
(6)滴定终点的判定依据是_______________。
