题目内容
14.下列各项操作中,错误的是( )| A. | 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 | |
| B. | 进行分液时,分液漏斗中的下层液体,从下端流出,上层液体则从上口倒出 | |
| C. | 萃取、分液前需对分液漏斗进行检漏 | |
| D. | 将上面的塞子拿下,可以保证分液漏斗内的液体顺利流出 |
分析 A.酒精与水混溶;
B.分液时应避免液体重新混合而污染;
C.分液漏斗用于盛装液体,且有活塞,应检漏;
D.分液时,为使液体顺利流出,应使漏斗内外压强相等.
解答 解:A.酒精与水混溶,不能用作萃取剂,应用苯或四氯化碳等,故A错误;
B.分液时应避免液体重新混合而污染,应使下层液体从下端流出,上层液体则从上口倒出,故B正确;
C.分液漏斗用于盛装液体,且有活塞,应检漏,故C正确;
D.分液时,为使液体顺利流出,应使漏斗内外压强相等,可将漏斗上面的塞子拿掉,故D正确.
故选A.
点评 本题考查较为综合,涉及物质的分离、提纯的实验操作,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握相关实验的操作方法,难度不大.

练习册系列答案
相关题目
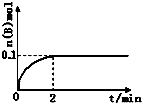
17.在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )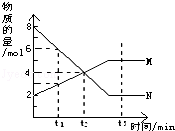

| A. | 反应的化学方程式为:2N?M | B. | t2时,正逆反应速率相等,达到平衡 | ||
| C. | t1时,N的浓度是M的浓度的3倍 | D. | t3时,正反应速率大于逆反应速率 |
5.在一定条件下,若要使反应CO(g)+NO2(g)?CO2(g)+NO(g)的反应速率增大可采取的措施有( )
| A. | 降低温度 | B. | 增大容器体积 | C. | 升高温度 | D. | 选用高效催化剂 |
2.下列反应中,不属于取代反应的是( )
| A. | 向苯酚中滴加浓溴水 | B. | 甲苯与浓硝酸、浓硫酸混合共热 | ||
| C. | 甲烷与氯气混合后见光 | D. | 乙醇与浓硫酸混合加热至170℃ |
9.根据转化关系判断下列说法正确的是( )


| A. | 反应③得到的乙酸乙酯中含有乙醇和乙酸,可用饱和氢氧化钠溶液除去 | |
| B. | 反应②中,1mol葡萄糖可生成3mol乙醇 | |
| C. | 将在空气中灼绕后的铜丝趁热插入乙醇中可得到乙酸 | |
| D. | 反应①中,(C6H10O5)n可表示淀粉或纤维素 |
19.下列实验装置或操作不符合实验要求的是( )
| A. | 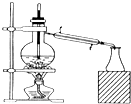 石油分馏 | B. | 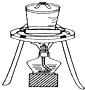 灼烧干海带 | ||
| C. | 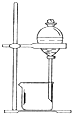 用CCl4提取碘水中的碘 | D. |  冶炼金属铁 |
3.下列关于溶液中的描述正确的是( )
| A. | 常温时,NaNO2溶液的pH=8,则该溶液中c(Na+)-c(NO2-)=9.9×10-7mol•L-1 | |
| B. | NaHSO4溶液与Ba(OH)2溶液反应至中性的离子方程式为:H++SO42++Ba2++OH-═BaSO4↓+H2O | |
| C. | 常温下物质的量浓度相等的下列四种溶液:①NH4HSO4;②CH3COONH4;③NH4Cl;④NH4Fe(SO4)2,四种溶液中c(NH4+)比较:②>①>④>③ | |
| D. | 常温下$\frac{Kw}{c({H}^{+})}$=1×10-10mol•L-1的溶液:Na+、K+、SiO32-、NO3-可以常量共存 |

 ;
; 结构(含E)的有13种;E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为
结构(含E)的有13种;E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为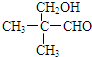 .
.