题目内容
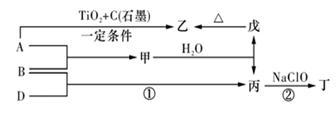
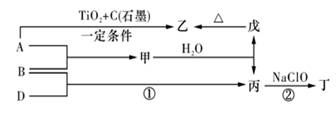
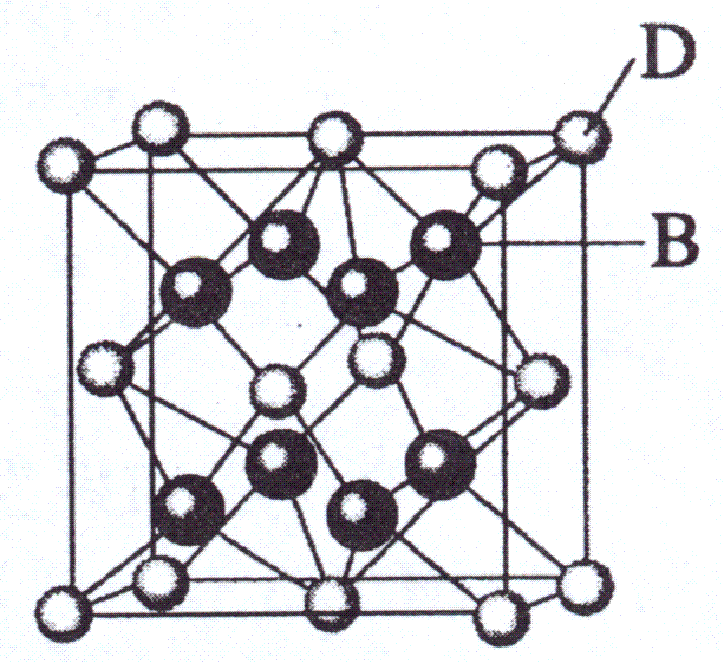
(11分) 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1―18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图。
请回答:
(1)A元素的名称是 ;
(2)B的元素符号是 ,C的元素符号是 ,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
(3)E属元素周期表中第 周期,第 族的元素,其元素名称是 , 它的+2价离子的电子排布式为 :
(4)从图中可以看出,D跟B形成的离子化合物的化学式为 ;该离子化合 物晶体的密度为ag?cm-3,则晶胞的体积是 (只要求列出算式)。

解析:从D、E是周期表中1―18列中E排第7列可判断E是第4周期VIIB族,所以D也在第4周期;图中离子化合物D:B=1:2,则D为Ca,且B的序数在前面,B为F,C为Cl;A与其他4种元素既不在同一周期又不在同一主族,所以A为H。
(2)考查氢键;
(3)锰在周期表中的位置,+2价时已经失去个电子,所以排布式为[Ar]3d5;
(4)ρ= ![]() = (40+38)×4÷(6.02×1023)g÷V = a g?cm-3
= (40+38)×4÷(6.02×1023)g÷V = a g?cm-3

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目