题目内容
能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,断开化学键要吸收能量,形成化学键要放出能量。已知拆开1 mol H-H键、1 mol I-I、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ。则由氢气和碘单质反应(H2+I2=2HI)生成1 mol HI需要 (填“放出”或“吸收”) ___ kJ的热量。
(2)在生产和生活中经常遇到化学能与电能的相互转化。
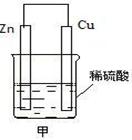
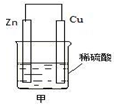
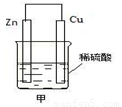
在如图甲装置中,负极电极反应式为 ,发生的是 反应(填“氧化”或“还原”,下同)。正极电极反应式为 ;总反应的离子方程式为 。
(3)若用氢氧化钾溶液做电解质溶液,用氢气做燃料,空气做氧化剂制成燃料电池,其负极反应式为 ;正极反应式为 。当有标状下2.24L氢气消耗时,另一极消耗氧气的物质的量为 。
(4)在如下图所示的原电池中,铝做 极,导线上电子由 极流向 极。
(12分)(1)放出;5.5
(2)Zn—2e—=Zn2+;氧化;2H++2e—=H2↑;Zn+2H+=Zn2++H2↑
(3)2H2—4e—+4OH—=4H2O;O2+4e—+2H2O=4OH—;0.05mol
(4)负;铝;镁(或负;正)
【解析】
试题分析:(1)反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以根据键能可知,该反应的反应热=436 kJ/mol+151 kJ/mol-299 kJ/mol×2=-11kJ/mol,所以生成1 mol HI需要放出5.5kJ的热量。
(2)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,则锌是负极,失去电子。铜是正极,溶液中的氢离子在正极得到电子,析出氢气。
(3)氢气在负极通入,由于溶液是碱性溶液,所以负极电极反应式是2H2—4e—+4OH—=4H2O;氧气在正极通入,电极反应式是O2+4e—+2H2O=4OH—;标准状况下2.24L氢气是0.1mol,失去0.2mol电子,所以根据电子的得失守恒可知,需要氧气的物质的量是0.2mol÷4=0.05mol。
(4)镁的金属性强于铝的,但能和氢氧化钠溶液反应的是铝,所以铝是负极,镁是正极,导线上电子由铝电极流向镁电极。
考点:考查反应热的计算、原电池的有关应用、判断和计算
点评:该题是高考中的常见题型,属于中等难度的试题,试题基础性强,贴近高考,旨在培养学生分析、归纳、总结问题的能力,有利于调动学生的学习兴趣,激发学生的学习积极性。该题的关键是明确原电池的工作原理,然后结合题意和装置图灵活运用即可。

 53随堂测系列答案
53随堂测系列答案