题目内容
I:能源是人类生活和社会发展的基础,地球上最基本的能源是
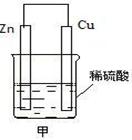
Ⅱ:理论上任意一个自发的氧化还原反应都能设计成原电池,现有如下反应:
2FeCl3+Cu=2FeCl2+CuCl2
如果将其设计成原电池,请写出负极材料及正极电极反应式.
负极材料:
III:工业上用电解熔融氧化铝的方法制取金属铝.
(1)请写出工业用电解熔融氧化铝制取铝的化学方程式:
(2)现冶炼2.7t 铝,需要转移电子的物质的量为
太阳能
太阳能
,大自然利用这一能源最成功的是植物的光合作用
植物的光合作用
.氢气被人们看作理想的绿色能源,己知氢气的热值是143kJ?g-1(热值指的是在一定条件下单位质量的物质完全燃烧所放出的热量,氢气转化为液态水.)请写出氢气燃烧的热化学方程式H2(g)+
O2(g)=H2O(1);△H=-286kJ?mol-1或2H2(g)+O2(g)=2H2O(l)△H=-572KJ?mol-1
| 1 |
| 2 |
H2(g)+
O2(g)=H2O(1);△H=-286kJ?mol-1或2H2(g)+O2(g)=2H2O(l)△H=-572KJ?mol-1
.| 1 |
| 2 |
Ⅱ:理论上任意一个自发的氧化还原反应都能设计成原电池,现有如下反应:
2FeCl3+Cu=2FeCl2+CuCl2
如果将其设计成原电池,请写出负极材料及正极电极反应式.
负极材料:
Cu
Cu
;正极电极反应式:2Fe3++2e-=2Fe2+
2Fe3++2e-=2Fe2+
.III:工业上用电解熔融氧化铝的方法制取金属铝.
(1)请写出工业用电解熔融氧化铝制取铝的化学方程式:
2Al2O3
4Al+3O2↑
| ||
2Al2O3
4Al+3O2↑
.
| ||
(2)现冶炼2.7t 铝,需要转移电子的物质的量为
3×105
3×105
mol.分析:Ⅰ:根据氢气的热值计算1mol氢气的燃烧热,进而书写热化学方程式;
Ⅱ:根据电池方程式结合化合价的变化判断正负极材料以及电极反应式,
Ⅲ:工业用电解熔融氧化铝制取铝的化学方程式为2Al2O3
4Al+3O2↑,根据化学方程式计算转移电子的物质的量.
Ⅱ:根据电池方程式结合化合价的变化判断正负极材料以及电极反应式,
Ⅲ:工业用电解熔融氧化铝制取铝的化学方程式为2Al2O3
| ||
解答:解:Ⅰ:地球上的能源主要来源于太阳能,通过植物的光合作用被循环利用,
由氢气的热值可知,1gH2燃烧放出的热量为143kJ,则1molH2放出的热量为:2×143kJ=286kJ,
所以氢气燃烧热的热化学方程式为H2(g)+
O2(g)=H2O(1);△H=-286kJ?mol-1或2H2(g)+O2(g)=2H2O(l)△H=-572KJ?mol-1,
故答案为:太阳能;植物的光合作用;H2(g)+
O2(g)=H2O(1);△H=-286kJ?mol-1或2H2(g)+O2(g)=2H2O(l)△H=-572KJ?mol-1;
Ⅱ:电池反应式为2FeCl3+Cu=2FeCl2+CuCl2,反应中Cu被氧化,应为原电池的负极,电极反应式为Cu-2e-=Cu2+,FeCl3在正极上得电子被还原,
电极反应式为2Fe3++2e-=2Fe2+,故答案为:Cu;Fe3++2e-=2Fe2+;
Ⅲ:(1)工业用电解熔融氧化铝制取铝的化学方程式为2Al2O3
4Al+3O2↑,故答案为:2Al2O3
4Al+3O2↑;
(2)2.7t 铝的物质的量为
=105mol,每生成1molAl转移的电子的物质的量为3mol,则冶炼2.7t 铝,需要转移电子的物质的量为3×105mol,故答案为:3×105.
由氢气的热值可知,1gH2燃烧放出的热量为143kJ,则1molH2放出的热量为:2×143kJ=286kJ,
所以氢气燃烧热的热化学方程式为H2(g)+
| 1 |
| 2 |
故答案为:太阳能;植物的光合作用;H2(g)+
| 1 |
| 2 |
Ⅱ:电池反应式为2FeCl3+Cu=2FeCl2+CuCl2,反应中Cu被氧化,应为原电池的负极,电极反应式为Cu-2e-=Cu2+,FeCl3在正极上得电子被还原,
电极反应式为2Fe3++2e-=2Fe2+,故答案为:Cu;Fe3++2e-=2Fe2+;
Ⅲ:(1)工业用电解熔融氧化铝制取铝的化学方程式为2Al2O3
| ||
| ||
(2)2.7t 铝的物质的量为
| 2.7×106g |
| 27g/mol |
点评:本题考查较为综合,涉及热化学方程式、原电池以及金属的电冶炼,题目难度不大,注意热化学方程式以及电极反应式的书写方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目