题目内容
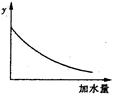
250C时,0.1mol·L-1稀醋酸加水稀释,如图中的纵坐标y可以是( )

| A.溶液的pH | B.醋酸的电离平衡常数 |
| C.溶液的导电能力 | D.醋酸的电离程度 |
C
试题分析:A、醋酸是弱电解质,加水稀释促进电离,氢离子的物质的量增大,溶液的体积也增大,0.1mol·L-1稀醋酸加水稀释,溶液体积增大为主,所以溶液中氢离子浓度逐渐减少,溶液的pH逐渐增大,但始终小于7,错误;B、温度不变,醋酸的电离平衡常数不变,错误;C、醋酸是弱电解质,加水稀释促进电离,氢离子的物质的量增大,溶液的体积也增大,0.1mol·L-1稀醋酸加水稀释,溶液体积增大为主,所以溶液中氢离子、醋酸根浓度逐渐减少,溶液的导电能力逐渐减小,正确;D、加水稀释促进醋酸电离,醋酸的电离程度增大,错误。

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案
相关题目
 H++A2-
H++A2-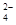 、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸锰(MnCO3)。其中一种工业流程如下:
、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸锰(MnCO3)。其中一种工业流程如下: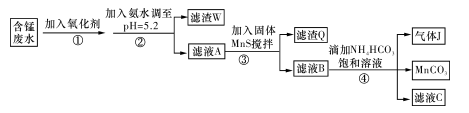
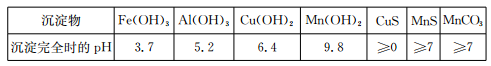

 增大
增大