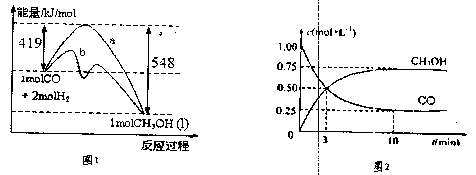题目内容
已知氟化氢气体存在下列平衡:2(HF)3 3(HF)2,(HF)2
3(HF)2,(HF)2 2HF;若平衡时混合气体的平均摩尔质量为42 g·mol -1,则(HF)3在平衡混合气中的体积分数为
2HF;若平衡时混合气体的平均摩尔质量为42 g·mol -1,则(HF)3在平衡混合气中的体积分数为
 3(HF)2,(HF)2
3(HF)2,(HF)2 2HF;若平衡时混合气体的平均摩尔质量为42 g·mol -1,则(HF)3在平衡混合气中的体积分数为
2HF;若平衡时混合气体的平均摩尔质量为42 g·mol -1,则(HF)3在平衡混合气中的体积分数为| A.小于10% | B.大于10% | C.等于10% | D.大于或等于10% |
B
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
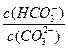 减小
减小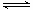 2C(g);△H<0。达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
2C(g);△H<0。达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是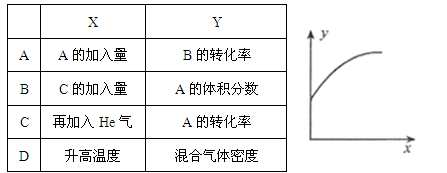
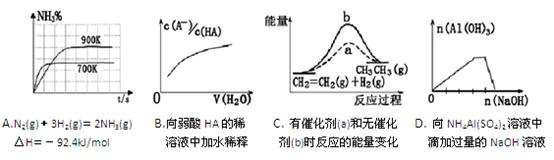
 ol N2的同时生成2n mol NH3
ol N2的同时生成2n mol NH3
 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
 平均相对分子质量不再改变
平均相对分子质量不再改变 量的2倍
量的2倍 ol H2,并使之进行反应: N2+3H2
ol H2,并使之进行反应: N2+3H2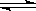 2NH3(放热反应),下列情况不能表明反应达到了平衡的是
2NH3(放热反应),下列情况不能表明反应达到了平衡的是 D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是
D(g)+E(g);△H>0 达到平衡后,下列说法中正确的是 CH3OH
CH3OH