题目内容
13.下列物质中所含原子数按从多到少的顺序排列正确的是( )①0.5mol NH3 ②标准状况下22.4L He ③4℃时18mL水 ④0.8mol H3PO4.
| A. | ①④③② | B. | ④③②① | C. | ②③④① | D. | ④③①② |
分析 利用N=n×NA,n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$来计算,并结合分子的构成即可解答.
解答 解:①0.5molNH3中的原子数为0.5×4×NA=2NA,
②标准状况下He的物质的量为$\frac{22.4L}{22.4L/mol}$=1mol,其原子数为l×1×NA=NA,
③水的质量为18mL×1g/mL=18g,其物质的量$\frac{18g}{18g/mol}$=1mol,则原子数为1×3×NA=3NA,
④0.8molH3PO4中的原子数为0.8×8×NA=6.4NA,
显然所含的原子数由多到少的顺序④③①②,
故选D.
点评 本题考查学生利用质量、体积来计算物质的量,并利用构成来分析原子数,明确计算公式及物质的构成是解答的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.对于反应Br2+SO2+2H2O=2HBr+H2SO4和2HBr+H2SO4(浓)=Br2+SO2↑+2H2O,下列说法中正确的是( )
| A. | 氧化性浓H2SO4>Br2,还原性:SO2>HBr | |
| B. | 它们互为可逆反应 | |
| C. | 反应条件的改变引起了反应方向的改变,它们都符合事实 | |
| D. | 它们相互矛盾,不可能符合事实 |
8.下列说法中正确的是( )
| A. | 2mol水的摩尔质量是1mol 水的摩尔质量的2倍 | |
| B. | 阿伏伽德罗常数就是6.02×1023 | |
| C. | 6.02×1023 mol-1叫做阿伏伽德罗常数 | |
| D. | 科学上规定含6.02×1023个粒子的任何粒子集合体计量为1mol |
18.下列说法正确的是( )
| A. | 水溶液中,1mol KCl和1mol KClO3电离出的氯离子一样多 | |
| B. | 电解质NaHCO3的电离方程式为:NaHCO3═Na++HCO3- | |
| C. | 凡溶于水后能电离出氢离子的化合物都是酸 | |
| D. | 氯化钠溶液在电流作用下,电离成自由移动的钠离子和氯离子 |
5.下列五个图中,横坐标表示加入的物质的量,纵坐标表示生成沉淀的量从A-E中选择各题要求的序号填入表中
| 溶液 | 加入的物质 | 答案序号 |
| 饱和石灰水 | 通CO2至过量 | |
| AlCl3溶液 | 通过量的NH3 | |
| 含少量NaOH的NaAlO2溶液 | 通过量的CO2 | |
| NaAlO2溶液 | 滴加稀HCl至过量 | |
| MgCl2 AlCl3的混和液 | 滴加NaOH至过量 |
| A. |  | B. | 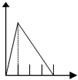 | C. | 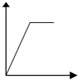 | D. |  | ||||
| E. |  |
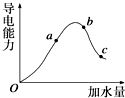 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答: