题目内容
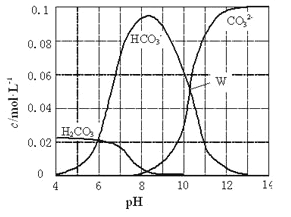
【题目】25℃时,0.1molNa2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH的关系如下图所示。下列有关溶液中离子浓度关系叙述正确的是
A. W点所示的溶液中:c (Na+)+c (H+)=2c(CO32- )+c (OH-)+c (Cl-)
B. pH=8的溶液中:c (H+)+c (H2CO3)+c (HCO3-)= c (OH-)+c (Cl- )
C. pH= 4的溶液中:c (H2CO3)+c (HCO3-)+c (CO32-)<0.1mol·L-1
D. pH=11的溶液中:c (Na+)>c (Cl-)>c (CO32- )>c (HCO3- )>c (H2CO3)
【答案】C
【解析】A.根据电荷守恒可知,溶液中离子应该满足关系式c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)+c(HCO3-),故A错误;B.根据图象可知pH=8时,溶液中碳酸氢钠的浓度远远大于碳酸钠的浓度,这说明反应中恰好是生成碳酸氢钠,则根据物料守恒可知c(H2CO3)+c(HCO3-)+c(CO32-)=c(Cl-)=![]() c(Na+),再由电荷守恒:c(Na+)+c(H+)=2c(CO32-)+ c(HCO3-)+c(OH-)+c(Cl-),则c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-),故B错误;C.pH=4,说明反应中有CO2生成,所以根据物料守恒可知c(H2CO3)+c(HCO3-)+c(CO32-)<0.1 molL-1,故C正确;D.根据图象可知pH=11时,溶液碳酸钠的浓度远远大于碳酸氢钠的浓度,这说明碳酸钠是过量的,则c(Na+)>c(CO32-)>c(Cl-)>c(HCO3-)>c(H2CO3),故D错误;故选C。
c(Na+),再由电荷守恒:c(Na+)+c(H+)=2c(CO32-)+ c(HCO3-)+c(OH-)+c(Cl-),则c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-),故B错误;C.pH=4,说明反应中有CO2生成,所以根据物料守恒可知c(H2CO3)+c(HCO3-)+c(CO32-)<0.1 molL-1,故C正确;D.根据图象可知pH=11时,溶液碳酸钠的浓度远远大于碳酸氢钠的浓度,这说明碳酸钠是过量的,则c(Na+)>c(CO32-)>c(Cl-)>c(HCO3-)>c(H2CO3),故D错误;故选C。

 阅读快车系列答案
阅读快车系列答案



