题目内容
【题目】现有下列五种物质:①CO2;②NH3;③SO2;④H2SO4;⑤NaCl。
(1)其中,能使品红溶液退色的是_____________(填序号,下同);
(2)属于电解质的是_____________ ;
(3)只含离子键的是________________;
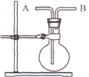
(4)利用下图装置并从B口进气,可收集的气体是___________ 。
【答案】 ③ ④⑤ ⑤ ②
【解析】(1)SO2能够使品红溶液褪色,加热后又会恢复原色,故能使品红溶液褪色的是③;(2)在水溶液中或熔化状态下能导电的化合物为电解质,则只有④H2SO4;⑤NaCl为电解质,①CO2;②NH3;③SO2本身不能电离,为非电解质,答案选④⑤;(4)利用下图装置并从B口进气,适合于气体密度小于空气的排气法收集,只有氨气的密度小于空气,二氧化硫和二氧化碳的密度均大于空气,故可用于收集的气体是氨气,答案选②。

练习册系列答案
相关题目
【题目】下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 将红色纸条放入到新制氯水中 | 纸条褪色 | 氯气有漂白性 |
B | 将硫酸酸化的H2O2溶液滴入到Fe(NO3)2溶液中 | 溶液变黄色 | H2O2氧化性比Fe3+强 |
C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 铝熔化且滴落下来 | 铝的熔点较低 |
D | 将NaI溶液加入到AgCl悬浊液中 | 产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
A. AB. BC. CD. D